1844試験 安全性
脊椎および寛骨(大腿骨近位部)の骨密度のベースラインからの変化率(安全性解析対象集団)(副次評価項目)(海外データ)
DXA法を用いて、ベースラインから投与48週までの脊椎および寛骨(大腿骨近位部)の骨密度の変化率を比較したところ、投与48週時点におけるベースラインからの変化率の平均値(標準偏差)は、脊椎では、ビクタルビ配合錠群が0.69%(3.13%)、ABC/DTG/3TC群が0.42%(3.00%)であり、寛骨(大腿骨近位部)では、ビクタルビ配合錠群が0.16%(2.21%)、ABC/DTG/3TC 群が0.30%(2.11%)でした。
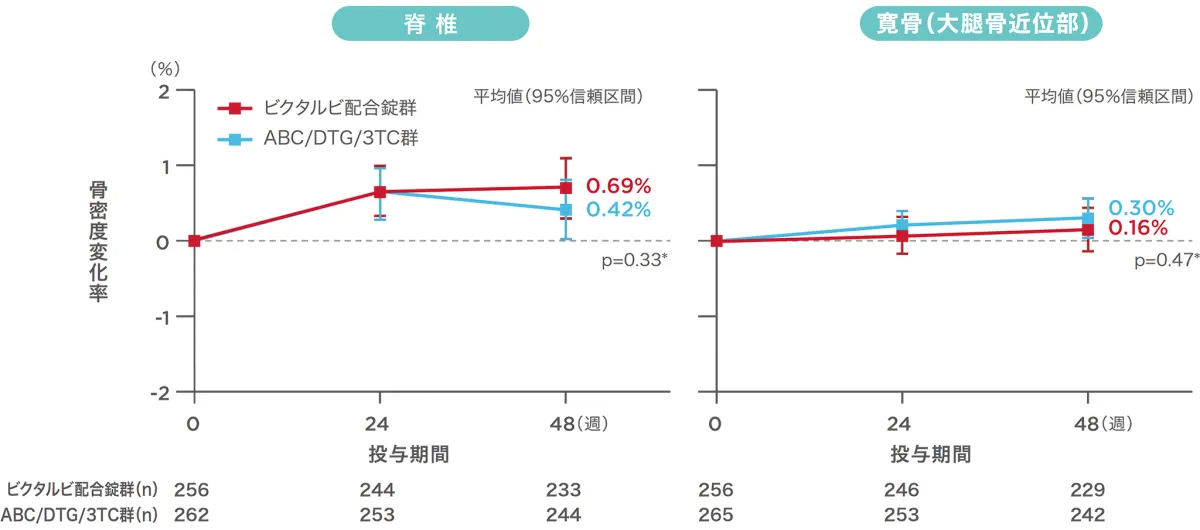
ABC:アバカビル、DTG:ドルテグラビル、3TC:ラミブジン、*:治療を固定効果として含むANOVA
Molina JM, et al.: Lancet HIV 2018; 5(7): e357.
社内資料(Phase 3 study : GS-US-380-1844)(承認時評価資料)
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者が含まれます。
有害事象および副作用の発現状況(安全性解析対象集団)(副次評価項目)
投与開始48週の副作用発現割合はビクタルビ配合錠群で8%、ABC/DTG/3TC群で16%であり、ビクタルビ配合錠群で有意に少ない割合でした。
重篤な副作用として、ビクタルビ配合錠群で脳血管発作1例が認められました。投与中止に至った副作用として、ビクタルビ配合錠群で頭痛2例、嘔吐、脳血管発作、異常な夢各1例が、ABC/DTG/3TC群で頭痛、そう痒症各1例が認められました。死亡はビクタルビ配合錠群で2例認められましたが、治験薬との関連は否定されました。
有害事象および副作用の発現割合(例数)は下表の通りです。
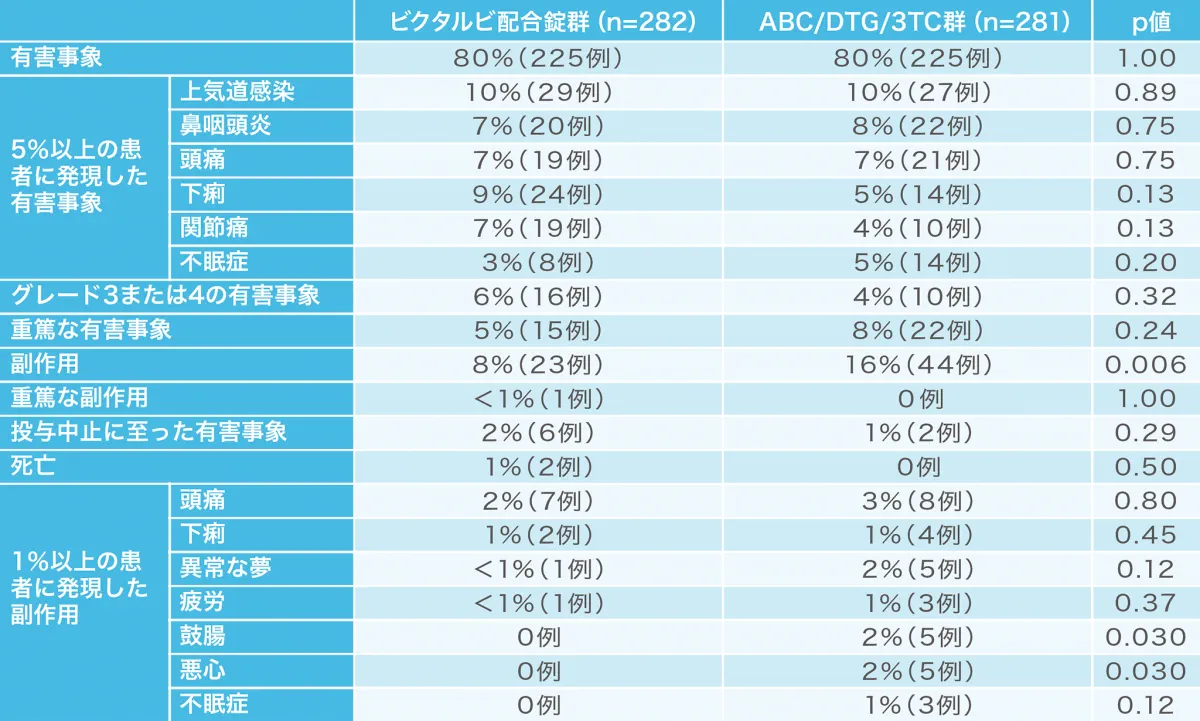
p値はFisherの正確確率検定による。
重篤な副作用として、ビクタルビ配合錠群で脳血管発作1例が認められた。投与中止に至った副作用として、ビクタルビ配合錠群で頭痛2例、嘔吐1例、脳血管発作1例、異常な夢1例、ABC/DTG/3TC群で頭痛1例、そう痒症1例が認められた。死亡はビクタルビ配合錠群で2例認められたが、治験薬との関連は否定された。
ABC:アバカビル、DTG:ドルテグラビル、 3TC:ラミブジン
Molina JM, et al.: Lancet HIV 2018; 5(7): e357.
Daar ES, et al.: Lancet HIV 2018; 5(7): e347.
社内資料(Phase 3 study : GS-US-380-1844)(承認時評価資料)
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者が含まれます。
腎機能:投与48週時点における腎バイオマーカー/尿中クレアチニン比 (安全性解析対象集団)(副次評価項目)(海外データ)
各群において、UACR、尿中RBP/クレアチニン比、尿中β2マイクログロブリン/クレアチニン比はベースラインから増加しました。
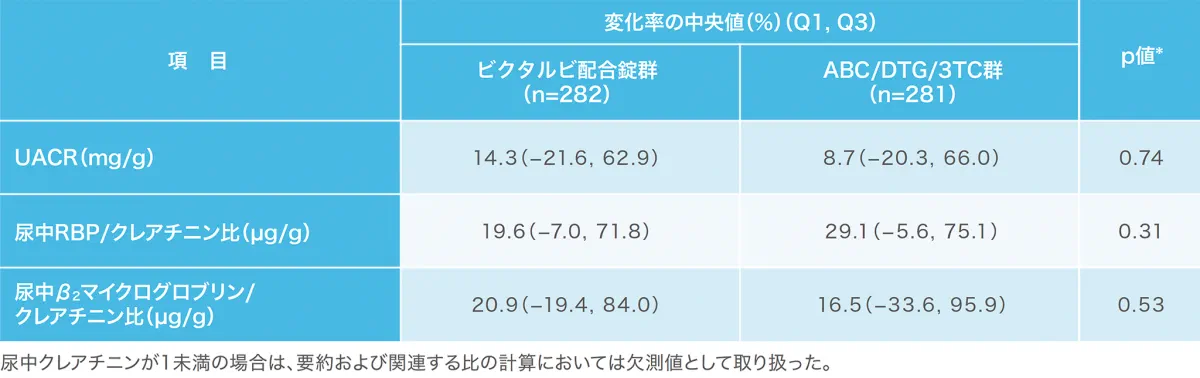
UACR:尿中アルブミン/クレアチニン比、RBP:レチノール結合蛋白、ABC:アバカビル、DTG:ドルテグラビル、3TC:ラミブジン
*:両側ウィルコクソンの順位和検定(ビクタルビ配合錠群 vs ABC/DTG/3TC群)
Molina JM, et al.: Lancet HIV 2018; 5(7): e357.
社内資料(Phase 3 study : GS-US-380-1844)(承認時評価資料)
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者が含まれます。
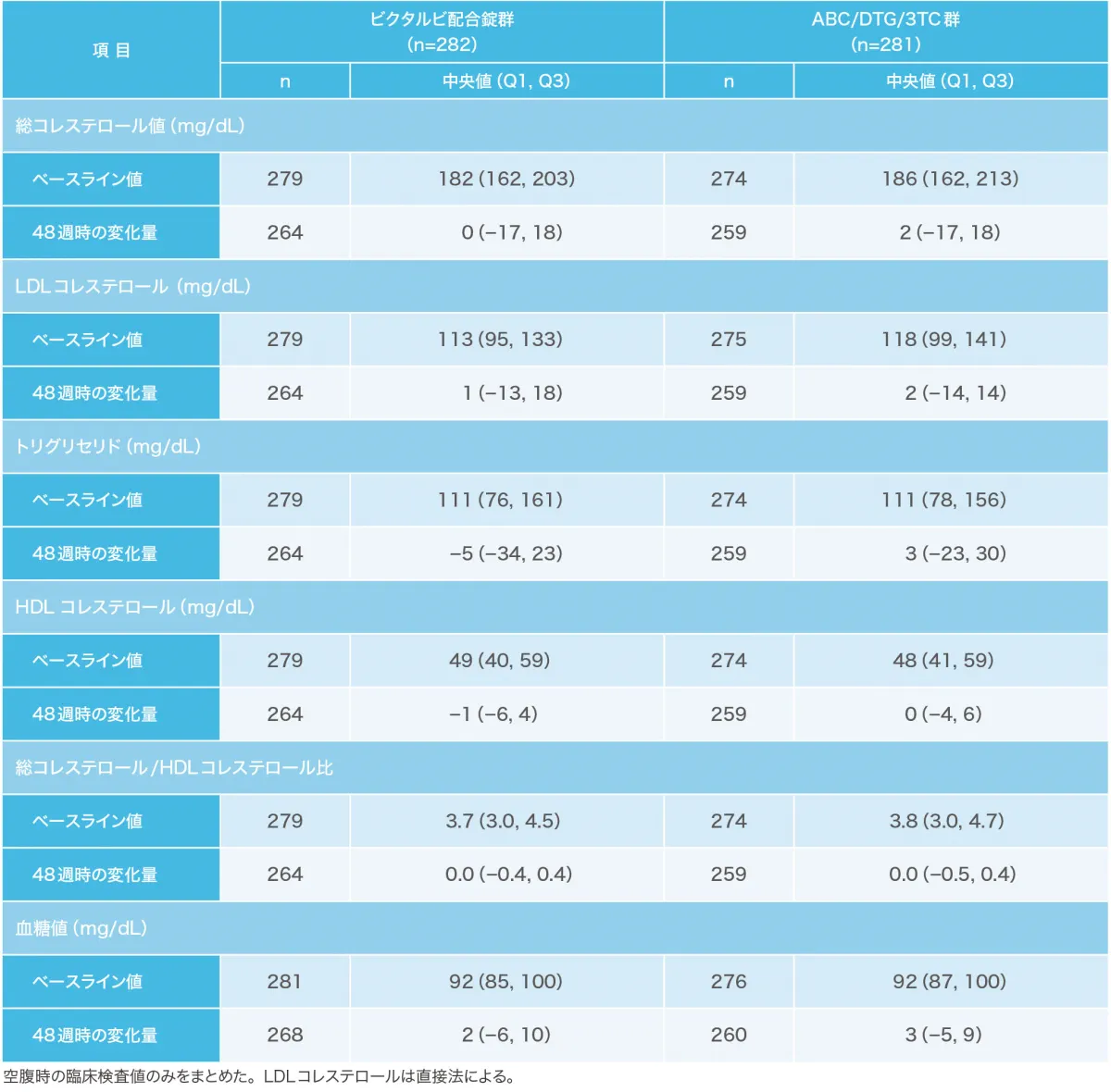
48週時における空腹時脂質・血糖パラメータのベースラインからの変化量 (安全性解析対象集団)(副次評価項目)(海外データ)