本剤の「警告・禁忌を含む使用上の注意」等については
注意事項等情報(電子化された添付文書)をご参照ください。
C型慢性肝炎又はC 型代償性肝硬変患者(ジェノタイプ1、2、4、5、6)を対象とした海外第3相臨床試験(ASTRAL-1:海外データ)
エプクルーサ配合錠を1日1回1錠、12週間服用することで、 C型慢性肝炎又はC型代償性肝硬変患者さんにおいてジェノタイプ、肝硬変および前治療歴の有無に関わらず、97.1%以上がSVR12を達成しました。また、624例中485例(77.7%)に有害事象が認められました。
試験概要
| 目的 | 未治療又はインターフェロン含有レジメンで治療歴のあるC型慢性肝炎又はC型代償性肝硬変を有する患者を対象にエプクルーサ配合錠12 週間投与の有効性と安全性を検討する。 |
|---|---|
| 対象 | C型慢性肝炎又はC型代償性肝硬変(ジェノタイプ1、2、4、5、6)を有する患者740例。 |
| 試験デザイン | 多施設共同、無作為化、二重盲検、プラセボ対照試験。 ジェノタイプ(1、2、4、6)及びC 型代償性肝硬変の有無により層別ランダム化した。ジェノタイプ5 のHCV感染被験者についてはランダム化せずにエプクルーサ配合錠12 週間投与群に組み入れた。前治療歴及びC 型代償性肝硬変を有する被験者の割合はそれぞれ約20% とした。 |
| 方法 | 対象をエプクルーサ配合錠投与群又はプラセボ投与群に無作為(5:1)に割り付け、食事の有無を問わず、1日1回1錠、12週間経口投与を行った。 |
| 主要評価項目 | SVR12率[投与終了から12週間後のHCV RNA量が定量下限(LLOQ)†未満を達成した患者割合]、安全性。 |
| 副次評価項目 | SVR4率、SVR24率、ウイルス学的治療不成功の患者の割合、投与期間中及び投与終了後のHCV RNA動態、SOF及びVELに対する耐性ウイルスの出現。 |
| 解析計画 | 主要評価項目はFull Analysis Set(FAS)においてSVR12 を達成した患者の割合(SVR12 率)とした。有意水準を0.05 とする両側正確1 標本二項検定により、閾値として設定した85%と比較し、目標値85%に対するエプクルーサ配合錠群の優越性の評価に用いた帰無仮説(H0)及び対立仮説(H1)は以下のとおりとした。 (H0:SVR12率=85%、H1:SVR12率≠85%) また、SVR12率のClopper-Pearson法に基づく点推定値及び正確な両側95%信頼区間(CI)をエプクルーサ配合錠群及びプラセボ群のそれぞれに対して算出した。 背景因子別のサブグループ解析は、ジェノタイプ/サブタイプ、C型代償性肝硬変の有無、HCV治療歴、等について実施することにした。 |
SVR:
sustained virologic response(持続的ウイルス陰性化)
†
定量下限(LLOQ):本試験のHCV RNA量の定量にはCOBAS® AmpliPrep /COBAS® TaqMan® HCV Quantitative Test
v2.0を用い、本分析法の定量下限(LLOQ)は15IU/mLでした。
◆ C型慢性肝炎又はC型代償性肝硬変を有する患者における海外第3相臨床試験(ASTRAL-1):試験デザイン
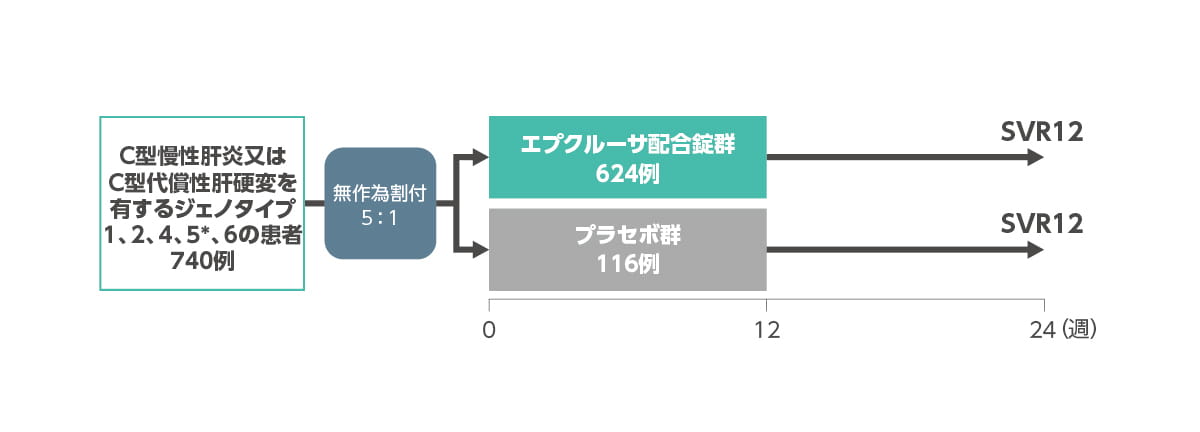
*ジェノタイプ5のHCV感染被験者についてはランダム化せずにエプクルーサ配合錠12週間投与群に組み入れた。
社内資料:承認時評価資料(海外第3相臨床試験:GS-US-342-1138)
Feld JJ, et al. N Engl J Med. 373(27): 2599-2607, 2015
[利益相反:本研究はギリアド・サイエンシズ, Inc. の資金提供および支援により行われた。本論文の著者には、ギリアド・サイエンシズ, Inc.の社員が含まれる。本論文の著者には、ギリアド・サイエンシズ, Inc.より講演料等を受領した者が含まれる。]
【用法・用量】(抜粋)
〈未治療又は前治療歴のないC型慢性肝炎又はC型代償性肝硬変におけるウイルス血症の改善〉
通常、成人には、1日1回1錠(ソホスブビルとして400mg 及びベルパタスビルとして100mg)を12 週間経口投与する。
患者背景
患者背景
| エプクルーサ配合錠群 (n=624) |
プラセボ群 (n=116) |
||
| 年齢中央値(範囲) | 56歳(18-82) | 55歳(25-74) | |
| 男性 | 374例(59.9%) | 68例(58.6%) | |
| BMI平均値(範囲)、 kg/m² | 26.7(16.9-56.9) | 25.9(17.9-40.2) | |
| 人種※1 | 白人 | 493例(79.0%) | 90例(77.6%) |
| 黒人 | 52例(8.3%) | 11例(9.5%) | |
| アジア人 | 62例(9.9%) | 11例(9.5%) | |
| その他 | 14例(2.2%) | 4例(3.4%) | |
| 不明 | 3例(0.5%) | 0例 | |
| IL28B 遺伝子型 | CC | 186例(29.8%) | 36例(31.0%) |
| CT | 339例(54.3%) | 53例(45.7%) | |
| TT | 94例(15.1%) | 26例(22.4%) | |
| 不明 | 5例(0.8%) | 1例(0.9%) | |
| C型代償性肝硬変※2 | 121例(19.4%) | 21例(18.1%) | |
| HCV RNA量(平均値±標準偏差) (log10IU/mL) HCV RNA ≧ 800,000 IU/mL |
6.3±0.66 461例(73.9%) |
6.3±0.58 87例(75.0%) |
|
| 前治療歴 | なし | 423例(67.8%) | 83例(71.6%) |
| あり | 201例(32.2%) | 33例(28.4%) | |
| 前治療 | PI+Peg-IFN+リバビリン | 56/201例(27.9%) | 6/33例(18.2%) |
| Peg-IFN+リバビリン | 122/201例(60.7%) | 24/33例(72.7%) | |
| IFN±リバビリン | 23/201例(11.4%) | 3/33例(9.1%) | |
| ジェノタイプ | 1a | 210例(33.7%) | 46例(39.7%) |
| 1b | 118例(18.9%) | 19例(16.4%) | |
| 2 | 104例(16.7%) | 21例(18.1%) | |
| 4 | 116例(18.6%) | 22例(19.0%) | |
| 5 | 35例(5.6%) | 0例 | |
| 6 | 41例(6.6%) | 8例(6.9%) | |
※1 自己申告。
※2 肝生検で確認、又はFibrotestスコア(>0.75)及びAPRI(>2)、又はFibroscan®の結果(>12.5kPa)。
社内資料:承認時評価資料(海外第3相臨床試験:GS-US-342-1138)
Feld JJ, et al. N Engl J Med. 373(27): 2599-2607, 2015
[利益相反:本研究はギリアド・サイエンシズ, Inc. の資金提供および支援により行われた。本論文の著者には、ギリアド・サイエンシズ, Inc.の社員が含まれる。本論文の著者には、ギリアド・サイエンシズ, Inc.より講演料等を受領した者が含まれる。]
SVR12率(主要評価項目、サブグループ解析)
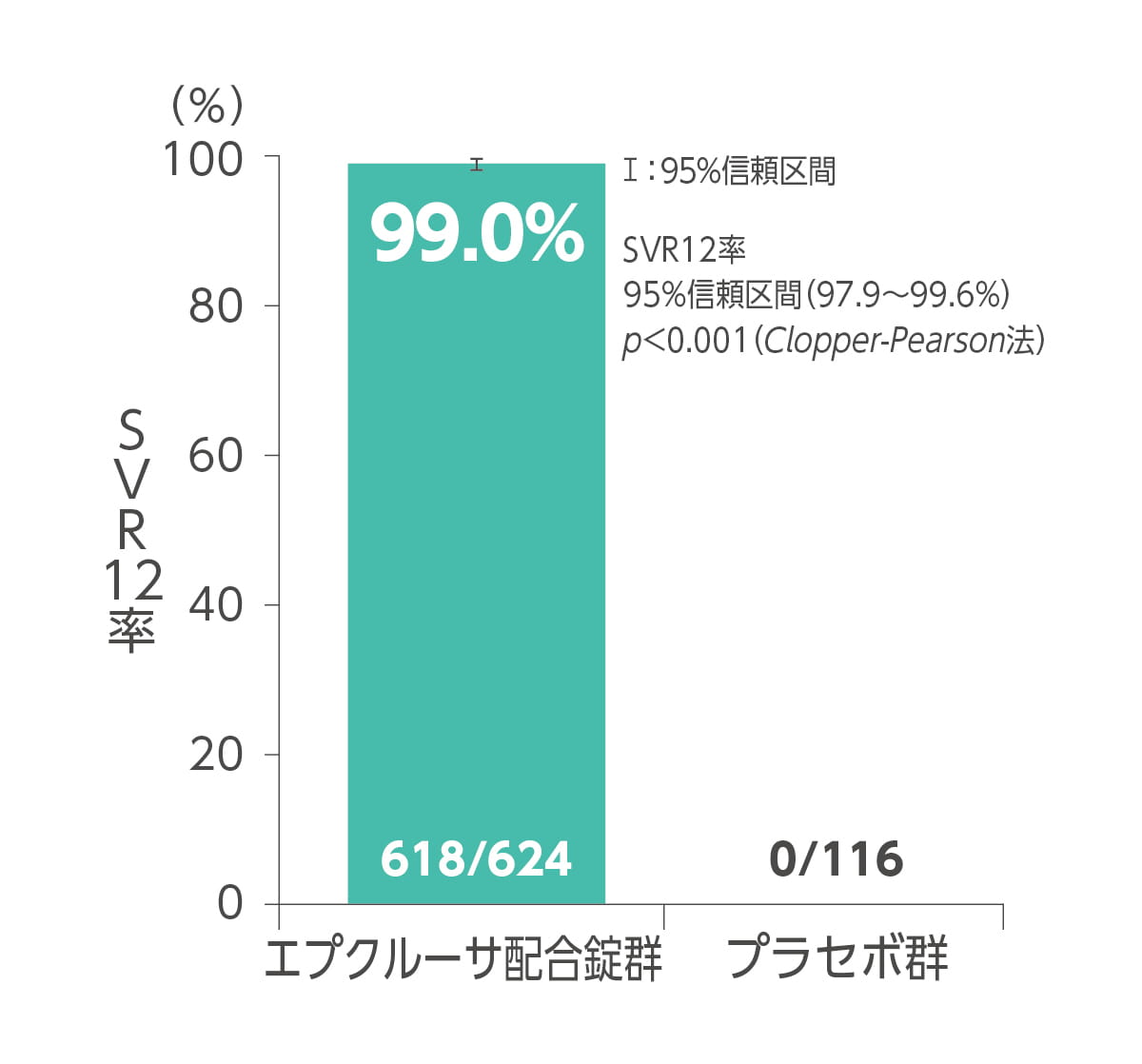
エプクルーサ配合錠12週間投与によるSVR12率(投与終了12 週間後のウイルス持続陰性化率)は99.0%(618/624 例:95%CI 97.9~99.6)でした。あらかじめ規定した85%の達成目標に対する統計学的有意性が示されました(p <>Clopper-Pearson法)(主要評価項目)。プラセボ群でSVR12を達成した被験者はいませんでした。
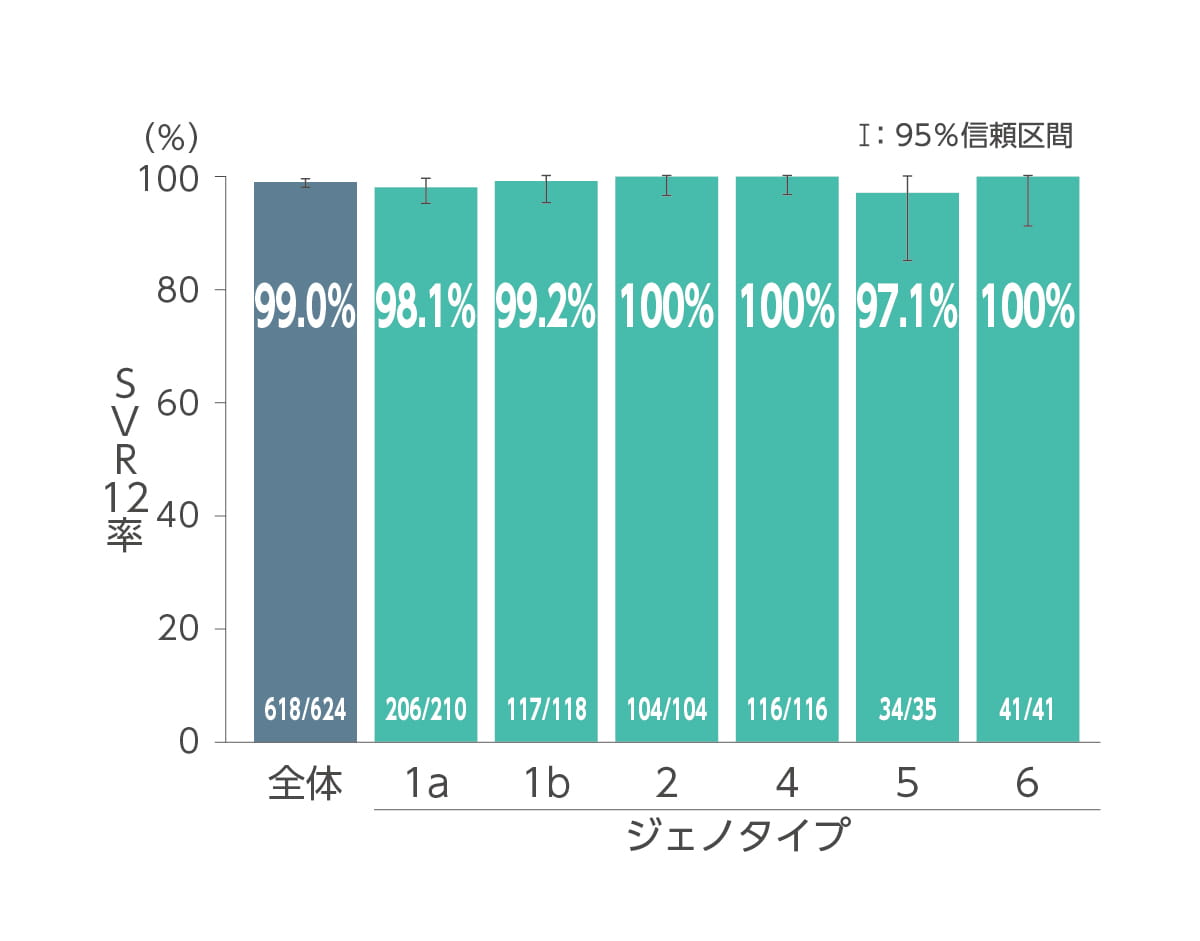
ジェノタイプ別SVR12 率は、ジェノタイプ1a が98.1%(206/210 例)、ジェノタイプ1b が99.2%(117/118例)、ジェノタイプ2が100.0%(104/104例)、ジェノタイプ4が100.0%(116/116例)、ジェノタイプ5が97.1%(34/35例)及びジェノタイプ6が100.0%(41/41例)でした(サブグループ解析)。
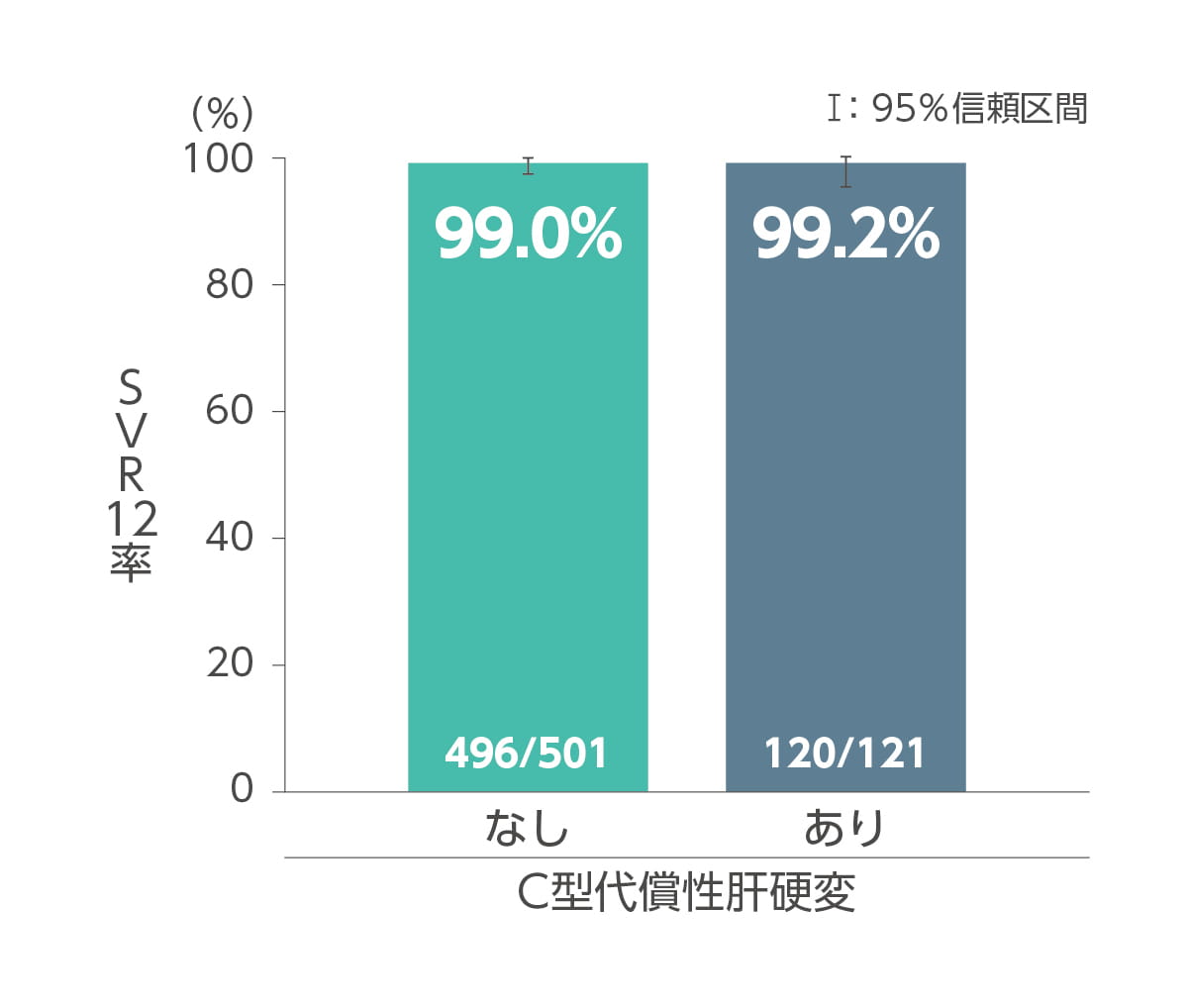
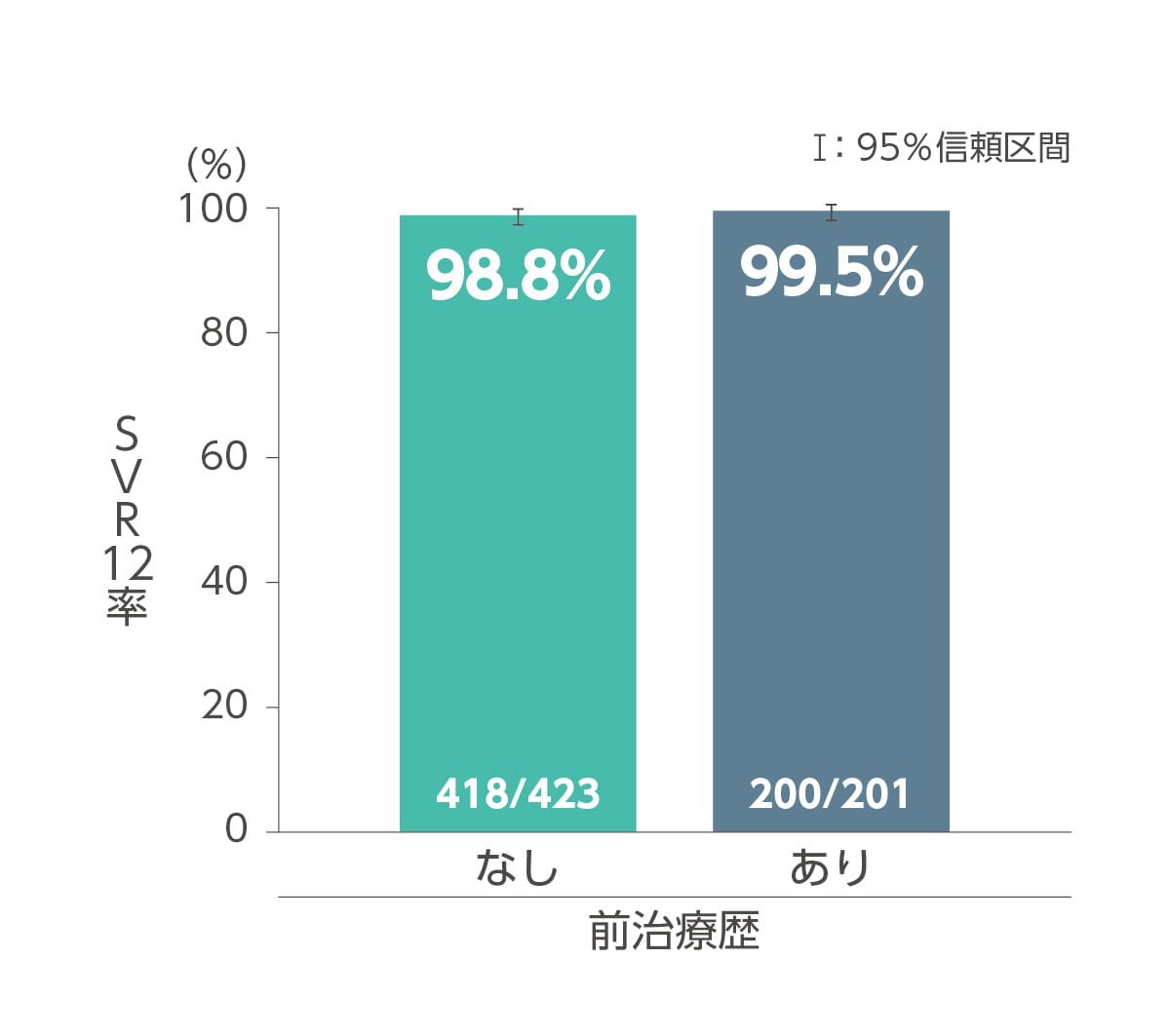
その他の背景因子別(C型代償性肝硬変の有無、前治療歴の有無)のSVR12率は以下のとおりです。
社内資料:承認時評価資料(海外第3相臨床試験:GS-US-342-1138)
Feld JJ, et al. N Engl J Med. 373(27): 2599-2607, 2015
[利益相反:本研究はギリアド・サイエンシズ, Inc. の資金提供および支援により行われた。本論文の著者には、ギリアド・サイエンシズ, Inc.の社員が含まれる。本論文の著者には、ギリアド・サイエンシズ, Inc.より講演料等を受領した者が含まれる。]
背景因子別SVR12率(サブグループ解析)
背景因子別SVR12率は以下の通りです。
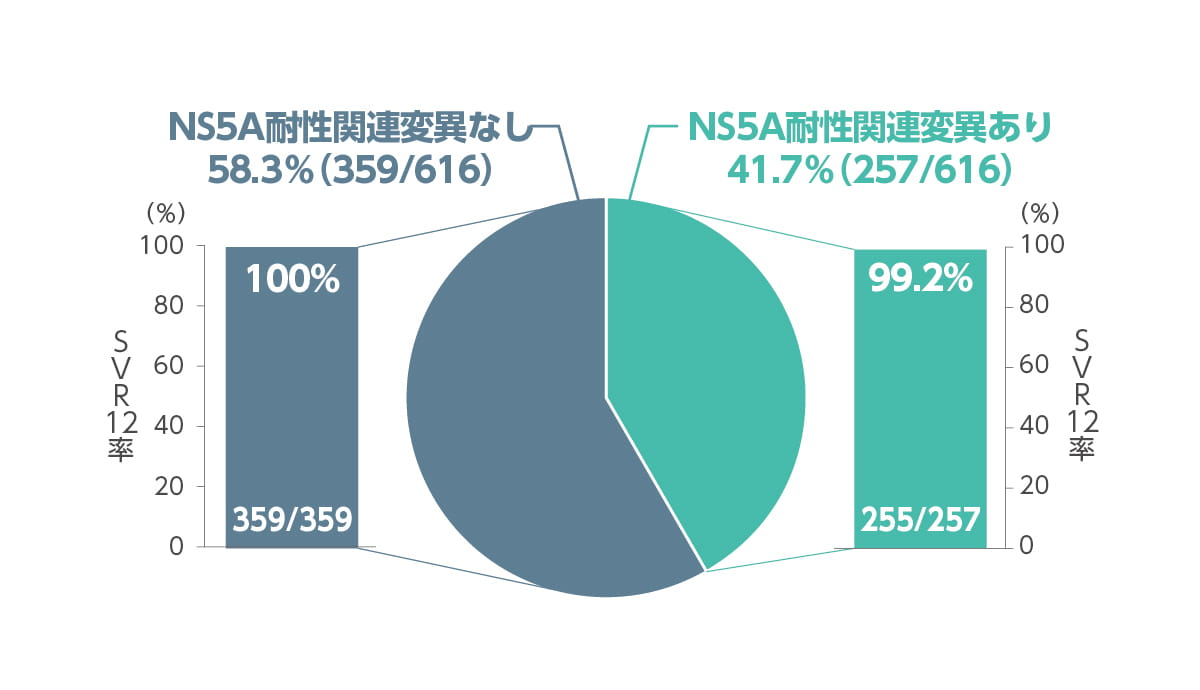
◆ ベースライン時のNS5A及びNS5B耐性関連変異の有無別SVR12率(サブグループ解析)
ベースライン時に41.7%(257/616例)でNS5A 耐性関連変異が認められました。エプクルーサ配合錠12週間投与により、NS5A耐性関連変異が検出された患者の99.2%(255/257例)がSVR12を達成しました。
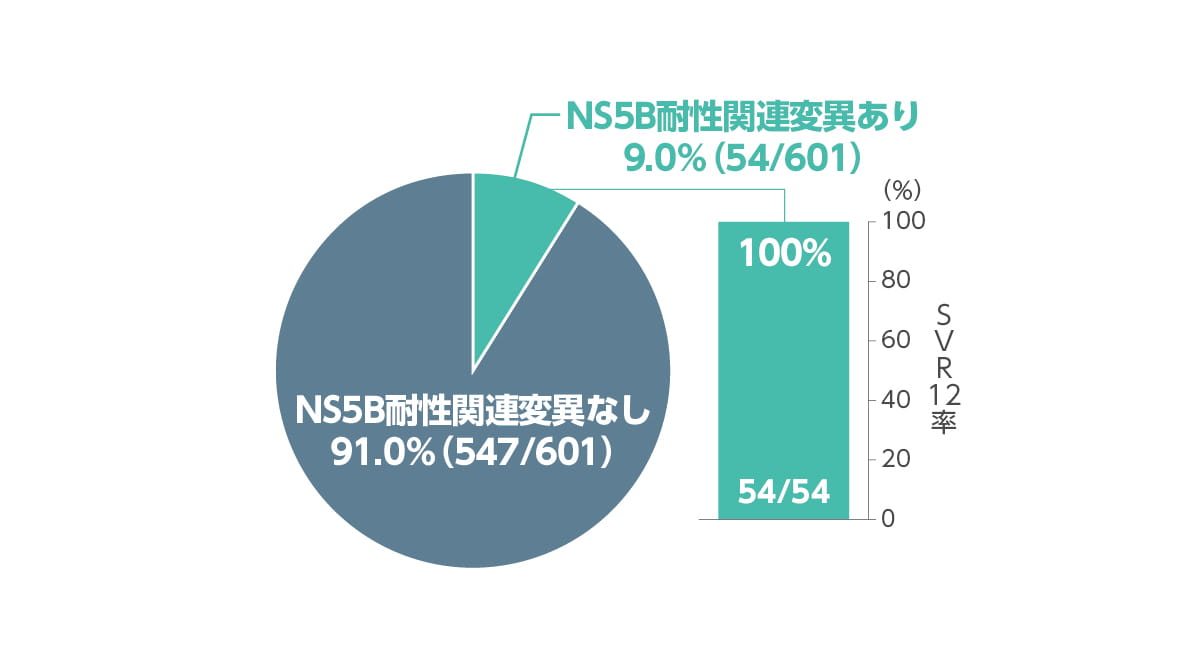
ベースライン時に9.0%(54/601例)でNS5B 耐性関連変異が認められました。これら54例全てでSVR12を達成しました。
◆ ベースライン時のNS5A耐性関連変異
| サブタイプ | NS5A耐性関連変異 | 例数 | 治療転帰 | |
| ジェノタイプ1 | 1a※1 (52例) |
K24R | 8 | SVR12達成 |
| M28V | 17 | SVR12達成 | ||
| Q30H | 1 | SVR12達成 | ||
| Q30R | 1 | 0/1例SVR12達成 | ||
| L31M | 6 | SVR12達成 | ||
| H58D | 1 | SVR12達成 | ||
| Y93F/L | 2 | SVR12達成 | ||
| Y93C | 1 | SVR12達成 | ||
| Y93H | 1 | SVR12達成 | ||
| Y93N | 1 | SVR12達成 | ||
| 複数変異 | 13 | 12/13例SVR12達成 | ||
| 1b (25例) |
L28M | 1 | SVR12達成 | |
| L31M | 5 | SVR12達成 | ||
| L31M/I | 1 | SVR12達成 | ||
| Y93H | 14 | SVR12達成 | ||
| 複数変異 | 4 | SVR12達成 | ||
| ジェノタイプ2 | 2a※2 (60例) |
L31M | 16 | SVR12達成 |
| T24S | 7 | SVR12達成 | ||
| 複数変異 | 37 | SVR12達成 | ||
| 2b (22例) |
K30R | 1 | SVR12達成 | |
| L31I/M | 1 | SVR12達成 | ||
| L31M | 20 | SVR12達成 | ||
| ジェノタイプ4 | (72例) | K24R | 2 | SVR12達成 |
| L28V | 1 | SVR12達成 | ||
| L28M | 10 | SVR12達成 | ||
| L30R | 42 | SVR12達成 | ||
| L30S | 1 | SVR12達成 | ||
| 複数変異 | 16 | SVR12達成 | ||
| ジェノタイプ5 | (6例) | Q30L | 1 | SVR12達成 |
| Q30R | 2 | SVR12達成 | ||
| P58S | 2 | SVR12達成 | ||
| T93S | 1 | SVR12達成 | ||
| ジェノタイプ6 | (22例) | F28M | 1 | SVR12達成 |
| F28V | 12 | SVR12達成 | ||
| F28M/V | 3 | SVR12達成 | ||
| T58A | 1 | SVR12達成 | ||
| T93S | 1 | SVR12達成 | ||
| 複数変異 | 4 | SVR12達成 |
※1 non-1a/1bを含む。
※2 non-2a/2bを含む。
◆ ベースライン時のNS5B耐性関連変異の有無別SVR12率
対象:ベースライン時に塩基配列決定データが得られた601例。
| サブタイプ | NS5B耐性関連変異 | 例数 | 治療転帰 | |
| ジェノタイプ1 | 1b (17例) |
N142T | 1 | SVR12達成 |
| L159F | 15 | SVR12達成 | ||
| V321A/I | 1 | SVR12達成 | ||
| ジェノタイプ2 | 2a※1 (3例) |
C/M289L/I | 3 | SVR12達成 |
| 2b (4例) |
E/N237G | 1 | SVR12達成 | |
| C/M289L/I | 3 | SVR12達成 | ||
| ジェノタイプ4 | (8例) | N142T | 1 | SVR12達成 |
| E/N237G | 7 | SVR12達成 | ||
| ジェノタイプ5 | (4例) | N142T | 2 | SVR12達成 |
| C/M289L/I | 2 | SVR12達成 | ||
| ジェノタイプ6 | (16例※2) | L159F | 1 | SVR12達成 |
| C/M289L/I | 16 | SVR12達成 | ||
| L320F/I/V | 1 | SVR12達成 |
※1 non-2a/2bを含む。
※2 複数変異例(M289L 及びL320F、L159F及び M289L)を含む。
社内資料:承認時評価資料(海外第3相臨床試験:GS-US-342-1138)
Feld JJ, et al. N Engl J Med. 373(27): 2599-2607, 2015
[利益相反:本研究はギリアド・サイエンシズ, Inc. の資金提供および支援により行われた。本論文の著者には、ギリアド・サイエンシズ, Inc.の社員が含まれる。本論文の著者には、ギリアド・サイエンシズ, Inc.より講演料等を受領した者が含まれる。]
SVR4率及びSVR24率(副次評価項目、サブグループ解析)
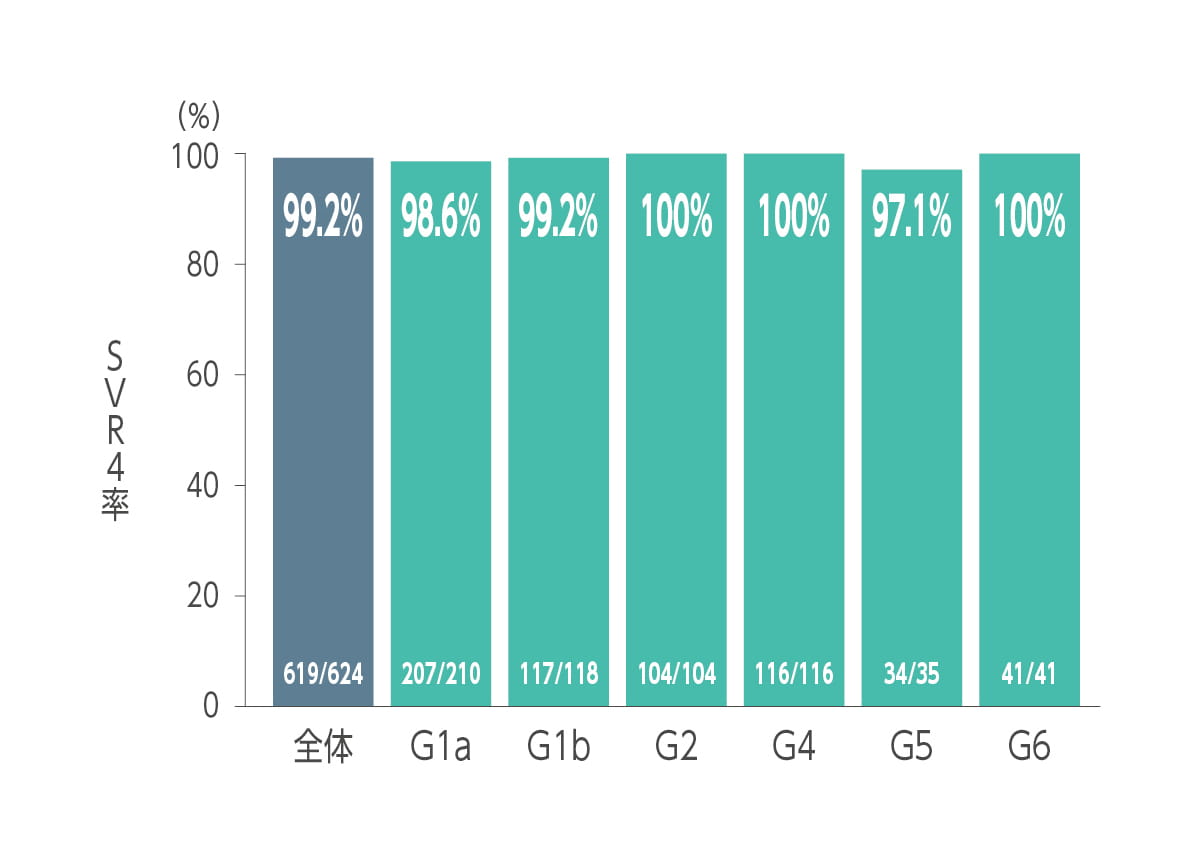
エプクルーサ配合錠12週間投与によるSVR4率(投与終了4 週間後のウイルス持続陰性化率)は99.2%(619/624例)でした(副次評価項目)。
ジェノタイプ別SVR4率は、ジェノタイプ1a が98.6%(207/210 例)、ジェノタイプ1b が99.2%(117/118 例)、ジェノタイプ2 が100%(104/104 例)、ジェノタイプ4 が100%(116/116 例)、ジェノタイプ5が97.1%(34/35例)及びジェノタイプ6が100%(41/41例)でした(サブグループ解析)。
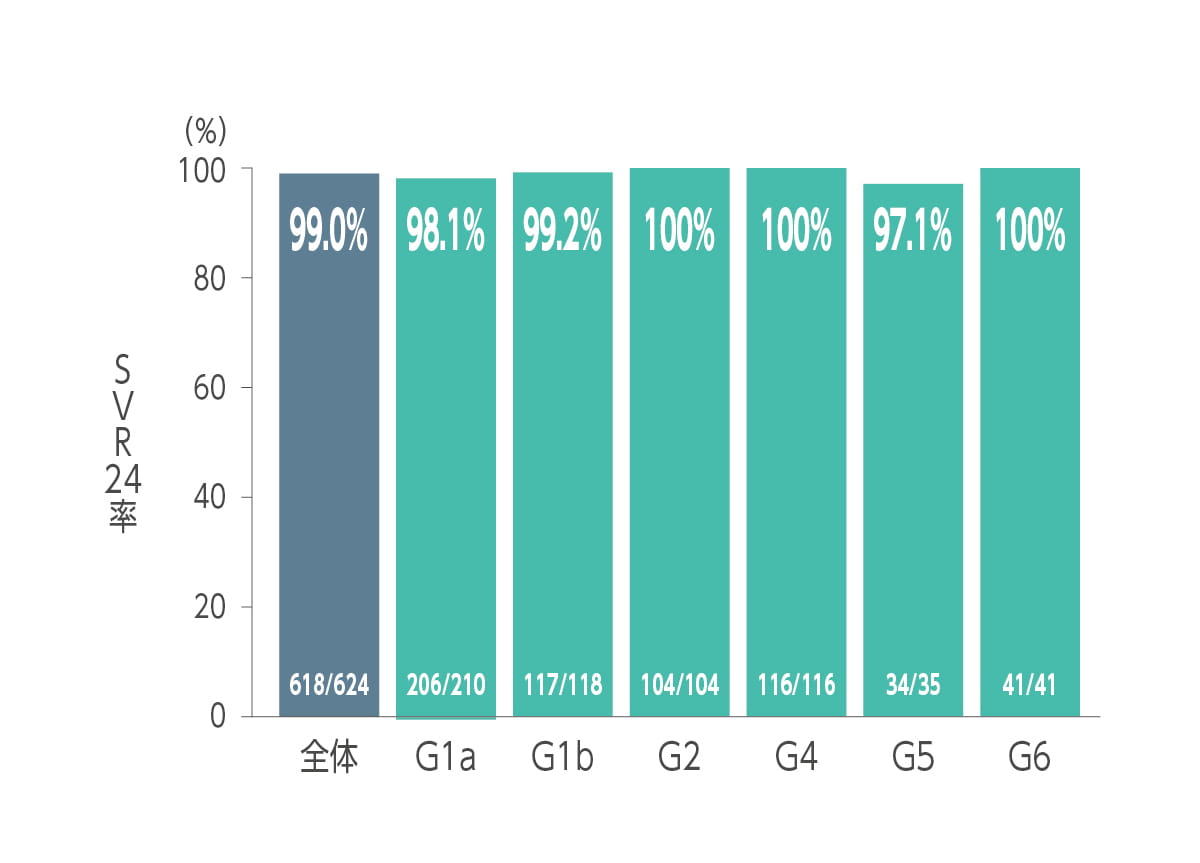
エプクルーサ配合錠12週間投与によるSVR24率(投与終了24 週間後のウイルス持続陰性化率)は99.0%(618/624例)でした(副次評価項目)。
ジェノタイプ別SVR24 率は、ジェノタイプ1a が98.1%(206/210 例)、ジェノタイプ1b が99.2%(117/118 例)、ジェノタイプ2 が100%(104/104 例)、ジェノタイプ4 が100%(116/116 例)、ジェノタイプ5が97.1%(34/35例)及びジェノタイプ6が100%(41/41例)でした(サブグループ解析)。
社内資料:承認時評価資料(海外第3相臨床試験:GS-US-342-1138)
Feld JJ, et al. N Engl J Med. 373(27): 2599-2607, 2015
[利益相反:本研究はギリアド・サイエンシズ, Inc. の資金提供および支援により行われた。本論文の著者には、ギリアド・サイエンシズ, Inc.の社員が含まれる。本論文の著者には、ギリアド・サイエンシズ, Inc.より講演料等を受領した者が含まれる。]
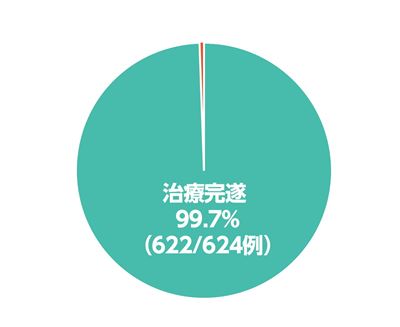
治療完遂率*(参考情報)
エプクルーサ配合錠投与例624 例中622例(99.7%)が12 週間の投与による治療を完遂しました。治療中止は有害事象(Grade 3 の不安)が1例、追跡不能が1例でした。
* 途中、中止することなく12週間、継続して服用した患者の割合。
社内資料:承認時評価資料(海外第3相臨床試験:GS-US-342-1138)
Feld JJ, et al. N Engl J Med. 373(27): 2599-2607, 2015
[利益相反:本研究はギリアド・サイエンシズ, Inc. の資金提供および支援により行われた。本論文の著者には、ギリアド・サイエンシズ, Inc.の社員が含まれる。本論文の著者には、ギリアド・サイエンシズ, Inc.より講演料等を受領した者が含まれる。]
ウイルス学的転帰(副次評価項目)
エプクルーサ配合錠12週間投与群で624例中6例(1.0%)がSVR12を達成しませんでした。2例は投与終了後4週に再燃が認められました(肝硬変のないHCV GT1aの未治療患者及び肝硬変を有するHCV GT1c/1hの前治療歴のある患者)。4 例(GT1:3 例、GT5:1 例)は、ウイルス学的治療不成功以外の理由によりSVR12を達成しませんでした(有害事象により投与13日に中止:1例、投与終了後12週に来院せず:2例、投与終了後4週の来院時までに死亡:1例)。投与終了後12週から24週に再燃を認めた患者はいませんでした。
安全性(主要評価項目)
【有害事象発現状況】
エプクルーサ配合錠投与群624 例中485 例(77.7%)に有害事象が認められました。主な有害事象は頭痛182 例(29.2%)、疲労126 例(20.2%)、咽頭炎79 例(12.7%)、悪心75 例(12.0%)等でした。1 例(0.2%)の死亡(就寝中の突然死)、1例(0.2%)の投与中止に至った有害事象(Grade3の不安)が認められました。重篤な有害事象は15 例(2.4% 左下肢膿瘍、左下肢蜂窩織炎、左下肢壊死、急性心筋梗塞、虫垂炎再燃、気管支炎、慢性閉塞性肺疾患、インフルエンザ、てんかん発作、胃腸炎、右腕の靭帯捻挫、肩回旋筋腱板症候群、躁病、動悸、小腸閉塞、上肢骨折、前庭神経炎、肺癌、就寝中の突然死 各1例)に認められました。
プラセボ投与群116 例中89 例(76.7%)に有害事象が認められました。主な有害事象は頭痛33 例(28.4%)、疲労23 例(19.8%)、悪心13 例(11.2%)、咽頭炎12 例(10.3%)等でした。死亡は認められず、2 例(1.7%)の投与中止に至った有害事象(ALT/AST 上昇)が認められました。重篤な有害事象は認められませんでした。
| エプクルーサ配合錠投与群 (n=624) |
プラセボ投与群 (n=116) |
|
|---|---|---|
| 有害事象による投与中止、例数(%) | 1(0.2%) | 2(1.7%) |
| 重篤な有害事象、例数(%) | 15(2.4%) | 0 |
| 死亡、例数(%) | 1(0.2%) | 0 |
| 有害事象発現例数(%) | 485(77.7%) | 89(76.7%) |
| 有害事象の種類、例数 (%) | ||
| 主な有害事象 | ||
| 頭痛 | 182(29.2%) | 33(28.4%) |
| 疲労 | 126(20.2%) | 23(19.8%) |
| 咽頭炎 | 79(12.7%) | 12 (10.3%) |
| 悪心 | 75(12.0%) | 13 (11.2%) |
| 不眠症 | 50(8.0%) | 11 (9.5%) |
| 下痢 | 48(7.7%) | 8 (6.9%) |
| 無力症 | 41(6.6%) | 9 (7.8%) |
| 関節痛 | 40(6.4%) | 9 (7.8%) |
| 咳嗽 | 39(6.3%) | 4 (3.4%) |
| 背部痛 | 29(4.6%) | 11 (9.5%) |
| 筋肉痛 | 25(4.0%) | 6 (5.2%) |
| 臨床検査値異常 | ||
| ヘモグロビン <10g> | 2(0.3%) | 0 |
| リンパ球数 350~500/mm³ | 3(0.5%) | 0 |
| 好中球数 500~750/mm³ | 4(0.6%) | 0 |
| 血小板数 25,000~50,000/mm³ | 1(0.2%) | 0 |
有害事象名は ICH 国際医薬用語集(MedDRA) Version 18.0 でコード化した。
社内資料:承認時評価資料(海外第3相臨床試験:GS-US-342-1138)
Feld JJ, et al. N Engl J Med. 373(27): 2599-2607, 2015
[利益相反:本研究はギリアド・サイエンシズ, Inc. の資金提供および支援により行われた。本論文の著者には、ギリアド・サイエンシズ, Inc.の社員が含まれる。本論文の著者には、ギリアド・サイエンシズ, Inc.より講演料等を受領した者が含まれる。]