1878試験 試験概要(海外データ)
GS-US-380-1878(1878試験)1-2
1: Daar ES, et al.: Lancet HIV 2018 ; 5(7): e347.
2: 社内資料(Phase 3 study : GS-US-380-1878)(承認時評価資料).
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者が含まれます。
| 目的 | 抗HIV薬による治療経験があり、ウイルス学的抑制が得られているHIV-1感染症患者を対象として、ブーストしたアタザナビル(ATV)またはダルナビル(DRV)+エムトリシタビン/テノホビル ジソプロキシルフマル酸塩(F/TDF)またはアバカビル/ラミブジン(ABC/3TC)からビクテグラビル/エムトリシタビン/テノホビル アラフェナミド(B/F/TAF:ビクタルビ配合錠)へ切り替えた場合の安全性および有効性を評価する。 |
|---|---|
| 対象 | スクリーニング前の6ヵ月以上にわたりリトナビル(RTV)またはコビシスタット(COBI)でブーストしたATVまたはDRV+F/TDFまたはABC/3TCのいずれかからなるレジメンによってウイルス学的抑制が得られている18歳以上のHIV-1感染症患者で次の条件を満たす577例 eGFRCG注1)が50mL/min以上、承認済みまたは治験中のインテグラーゼ阻害薬の使用歴がない、F、テノホビル、ABCまたは3TCに対する耐性の記録または疑いがない。 |
| 試験方法 | 多施設共同無作為化非盲検実薬対照試験(国際共同治験) |
| 投与方法 | 対象患者を以下の2投与群のいずれかに1:1の比率で割り付けた。 ビクタルビ配合錠群:ビクタルビ配合錠(B 50mg/F 200mg/TAF 25mg)への切り替え(食事に関係なく1日1回経口投与) ATVまたはDRVを含むレジメンの継続投与群:RTVまたはCOBIでブーストしたATVまたはDRV+F/TDFまたはABC/3TCのいずれかからなる現在のレジメンの継続(1日1回食後に投与) 無作為化の層別化は、スクリーニング時における過去の治療レジメン群[TDFを含むレジメン(RTVまたはCOBIでブーストしたATVまたはDRV+F/TDF)およびTDFを含まないレジメン(RTVまたはCOBIでブーストしたATVまたはDRV+ABC/3TC)]に基づいて行った。 |
| 主要評価項目 | FDAのスナップショットアルゴリズムによる投与48週時点の血漿中HIV-1 RNA量が50 copies/mL以上の被験者の割合に基づき、ビクタルビ配合錠に切り替えた場合とブーストしたATVまたはDRV+F/TDFまたはABC/3TCのいずれかからなるレジメンを継続した場合の有効性の比較評価(非劣性) |
| 副次評価項目 | FDAのスナップショットアルゴリズムによる投与48週時点の血漿中HIV-1 RNA量が50 copies/mL未満および20 copies/mL未満の被験者の割合、投与48週時点のCD4細胞数のベースラインからの変化量、投与48週までの2投与群間での安全性および忍容性(有害事象の発現状況、腎機能、脂質・血糖パラメータ)の評価 |
| 解析計画 | 主要評価項目における実薬対照に対するビクタルビ配合錠の非劣性は、投与群間差(ビクタルビ配合錠群−ATVまたはDRVを含むレジメンの継続投与群)の95.002%信頼区間の上限値が、事前に設定した非劣性マージン4%を上回らない場合と定義した。投与群間差およびその95.002%信頼区間は、2つの逆向きの片側検定を用い、条件付けを行わない正確法に基づき算出した。 |
注1) Cockcroft-Gault式による推算糸球体ろ過量
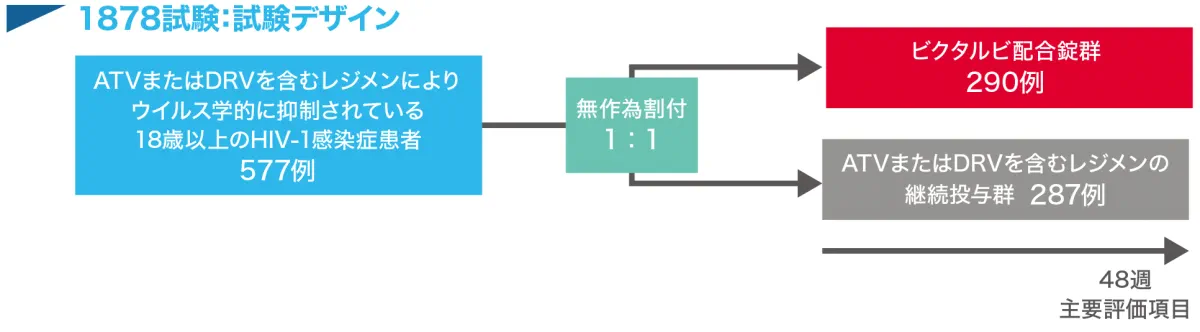
無作為割り付けされ、治験薬を少なくとも1回投与された577例(ビクタルビ配合錠群290例、ATVまたはDRVを含むレジメンの継続投与群287例)を最大の解析対象集団(FAS)および安全性解析対象集団とした。
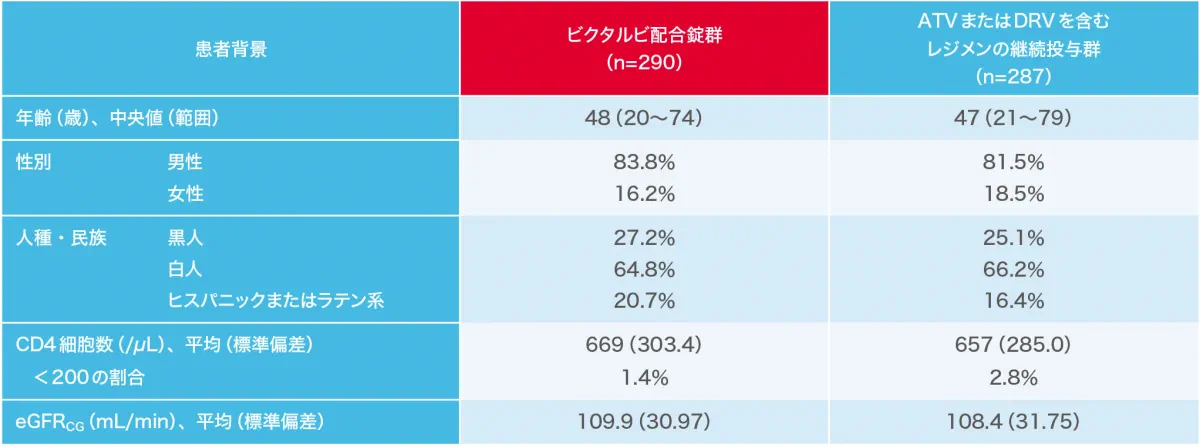
1878試験の患者背景