4030試験 試験概要(海外データ)
GS-US-380–4030(4030試験)1
1:Sax PE, et al.: Clin Infec Dis 2021;73(2): e485-e493.
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者、ギリアド・サイエンシズ社の社員である者が含まれます。
| 目的 | 抗HIV薬による治療経験があり、ウイルス学的抑制が得られているHIV-1感染症患者を対象として、ドルテグラビル(DTG)+エムトリシタビン/テノホビル アラフェナミド(F/TAF)またはエムトリシタビン/テノホビル ジソプロキシルフマル酸塩(F/TDF)から、ビクテグラビル/エムトリシタビン/テノホビル アラフェナミド(B/F/TAF:ビクタルビ配合錠)またはDTG+F/TAFへ切り替えた場合の安全性および有効性を評価する。 |
|---|---|
| 対象 | DTG+F/TAFまたはF/TDFによってウイルス学的抑制が得られている18歳以上のHIV-1感染症患者で次の条件を満たす565例 NRTI耐性変異ありまたは疑われる場合は6ヵ月以上、NRTI耐性変異なしまたは疑われない場合は3ヵ月以上のウイルス抑制(血漿HIV-1 RNA 50 copies/mL未満)、INSTI耐性変異なし、INSTIを含むレジメンにてウイルス学的失敗なし、eGFRCG注1)が50mL/min以上、妊娠検査にて陰性かつ有効な避妊法の使用 |
| 試験方法 | 多施設共同無作為化二重盲検実薬対照並行群間非劣性試験(国際共同治験) |
| 投与方法 | 対象患者を以下の2投与群のいずれかに1:1の比率でランダムに割り付けた。 ビクタルビ配合錠群:ビクタルビ配合錠(B 50mg/F 200mg/TAF 25mg)およびDTGに対応したプラセボおよびF/TAFのFDC注2)に対応したプラセボを食事に関係なく1日1回経口投与 DTG+F/TAF群:DTG 50mg+F/TAF(F 200mg/TAF 25mg)のFDCおよびビクタルビ配合錠に対応したプラセボを食事に関係なく1日1回経口投与 |
| 評価項目 | 主要評価項目:FDAのスナップショットアルゴリズムによる投与48週時点の血漿中HIV-1 RNA量が50
copies/mL以上の被験者の割合に基づき、DTG+F/TAFまたはF/TDFのレジメンからビクタルビ配合錠に切り替えた場合とDTG+F/TAFに切り替えた場合の有効性の比較評価(非劣性)。 副次評価項目:FDAのスナップショットアルゴリズムによる投与48週時点の血漿中HIV-1 RNA量が50 copies/mL未満の被験者の割合、投与48週時点のCD4細胞数のベースラインからの変化量、投与48週までの2投与群間での安全性および忍容性(有害事象の発現状況、脂質パラメータ)の評価等 |
| 解析計画 | 主要評価項目:実薬対照に対するビクタルビ配合錠の非劣性は、投与群間差(ビクタルビ配合錠群-DTG+F/TAF群)の95.001%信頼区間の上限値が、事前に設定した非劣性マージン4%を上回らない場合と定義した。投与群間差およびその95.001%信頼区間は、2つの逆向きの片側検定を用い、条件付けを行わない正確法に基づき算出した。 |
注1) Cockcroft-Gault式による推算糸球体ろ過量
注2)固定用量配合錠
4030試験:試験デザイン
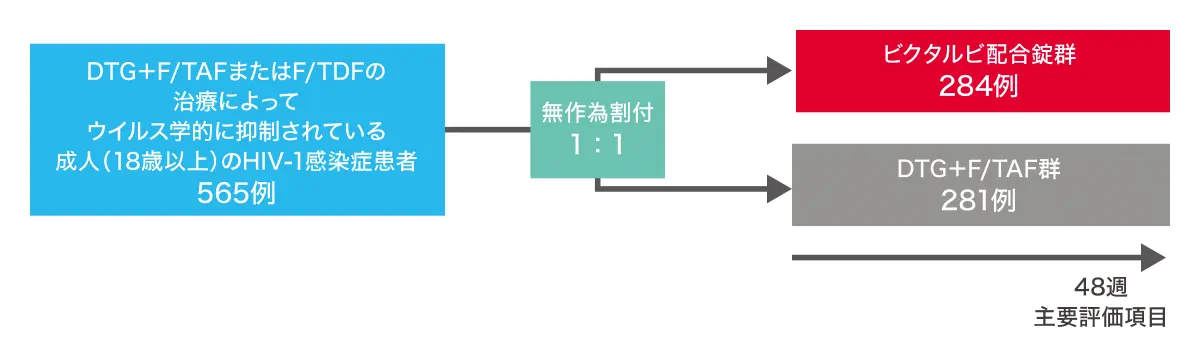
無作為割り付けされ、治験薬を少なくとも1回投与された565例(ビクタルビ配合錠群284例、DTG+F/TAF群281例)を最大の解析対象集団(FAS)および安全性解析対象集団とした。
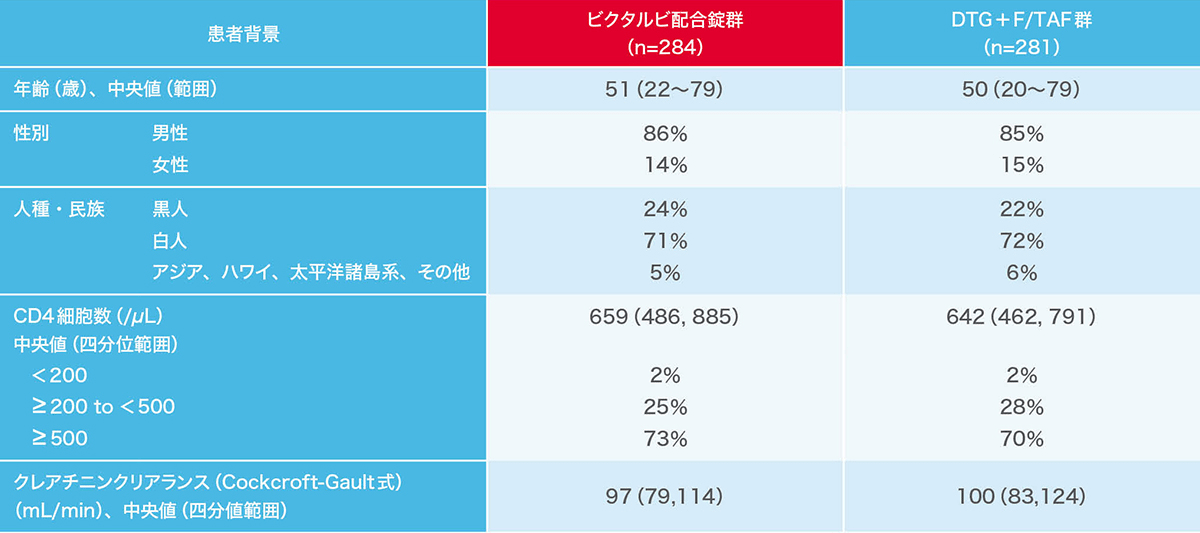
4030試験の患者背景