4030試験 安全性
有害事象および副作用の発現状況(安全性解析対象集団)(副次評価項目)(海外データ)
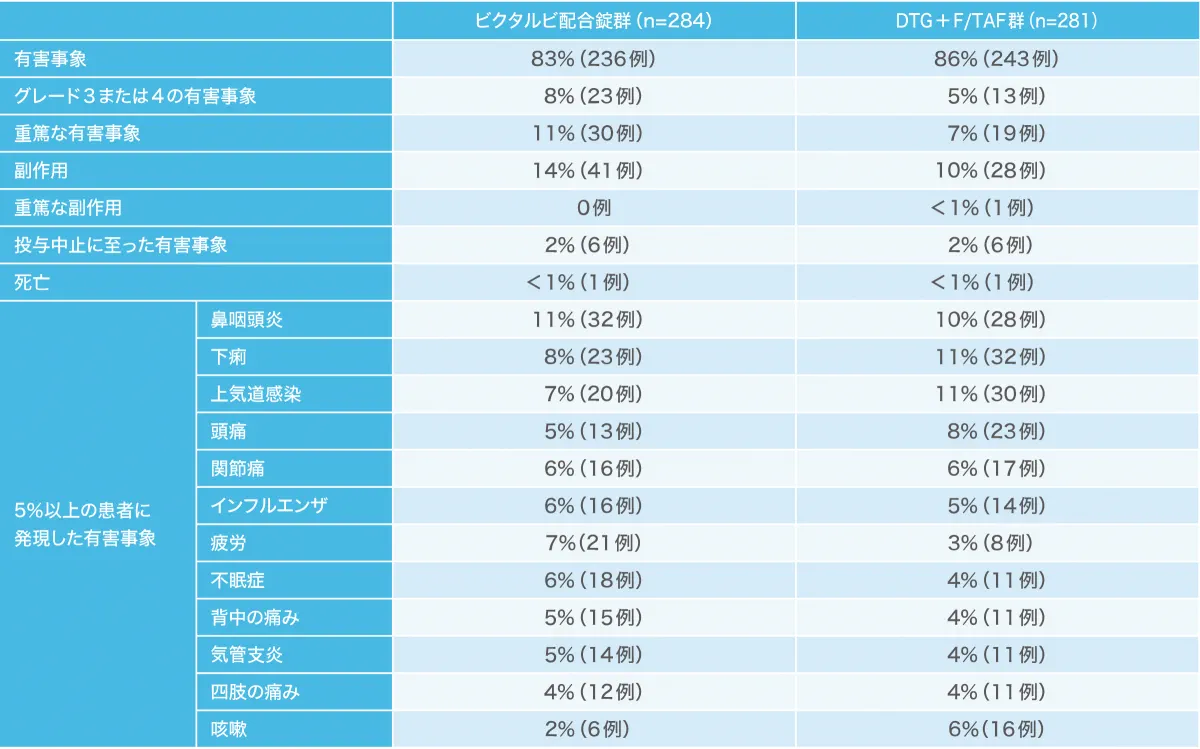
投与48週時点で、ビクタルビ配合錠群で284例中41例(14.0%)、DTG+F/TAF群で281例中28例(10.0%)に副作用が認められました。5%以上の患者に発現した有害事象は、ビクタルビ配合錠群で鼻咽頭炎32例(11.0%)、下痢23例(8.0%)等、DTG+F/TAF群で下痢32例(11.0%)、上気道感染30例(11.0%)等でした。
重篤な有害事象は、ビクタルビ配合錠群で憩室炎2例、胆道ジスキネジア、気管支痙攣、心肺停止、蜂巣炎、胸痛、胆嚢炎、慢性閉塞性肺疾患、鎖骨骨折、脳振盪、冠動脈疾患、医療機器関連感染、薬物乱用、呼吸困難、消化管内異物、胃腸炎、感染性下痢、大腸穿孔、靱帯断裂、腰部脊柱管狭窄症、肺の悪性新生物、過量投与、直腸周囲膿瘍、肺炎、肺臓炎、気胸、処置後感染、腎盂腎炎、リバウンド精神病、横紋筋融解症、痙攣発作、洞性頻脈、腱断裂、心室性頻脈 各1例、DTG+F/TAF群で腹痛、狭心症、足関節部骨折、虫垂炎、血中ブドウ糖増加、胆嚢炎、急性胆嚢炎、憩室炎、呼吸困難、鼡径ヘルニア、リスフラン骨折、心筋梗塞、骨壊死、腎盂腎炎、硬膜下血腫、椎骨動脈解離、ウイルス性上気道感染、嘔吐、卵黄嚢腫瘍(部位不明)各1例が認められました。
投与中止に至った有害事象は、ビクタルビ配合錠群で疲労、医療機器関連感染、消化不良、疲労および悪夢および多汗症、異常な夢、激越で各1例(医療機器関連感染を除いて治験薬と関連があると考えられた)、DTG+F/TAF群で不眠症および疲労および頭痛および悪心および不安、全身性皮疹、斑状丘疹状皮疹および結膜充血、無力症および鼓腸、卵黄嚢腫瘍(部位不明)、異常な夢および睡眠障害で各1例(不安、全身性皮疹、卵黄嚢腫瘍を除いて治験薬と関連があると考えられた)が認められました。死亡はビクタルビ配合錠群で1例(事象について論文に記載なし)とDTG+F/TAF群で心筋梗塞による1例(治験薬との関連性は評価できず)が認められました。
有害事象及び副作用の発現割合(例数)は下表のとおりです。
1: Sax PE, et al.: Clin Infec Dis 2021; 73(2): e485-e493.
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者、ギリアド・サイエンシズ社の社員である者が含まれます。
空腹時脂質パラメータのベースラインからの変化量(安全性解析対象集団)(副次評価項目)(海外データ)
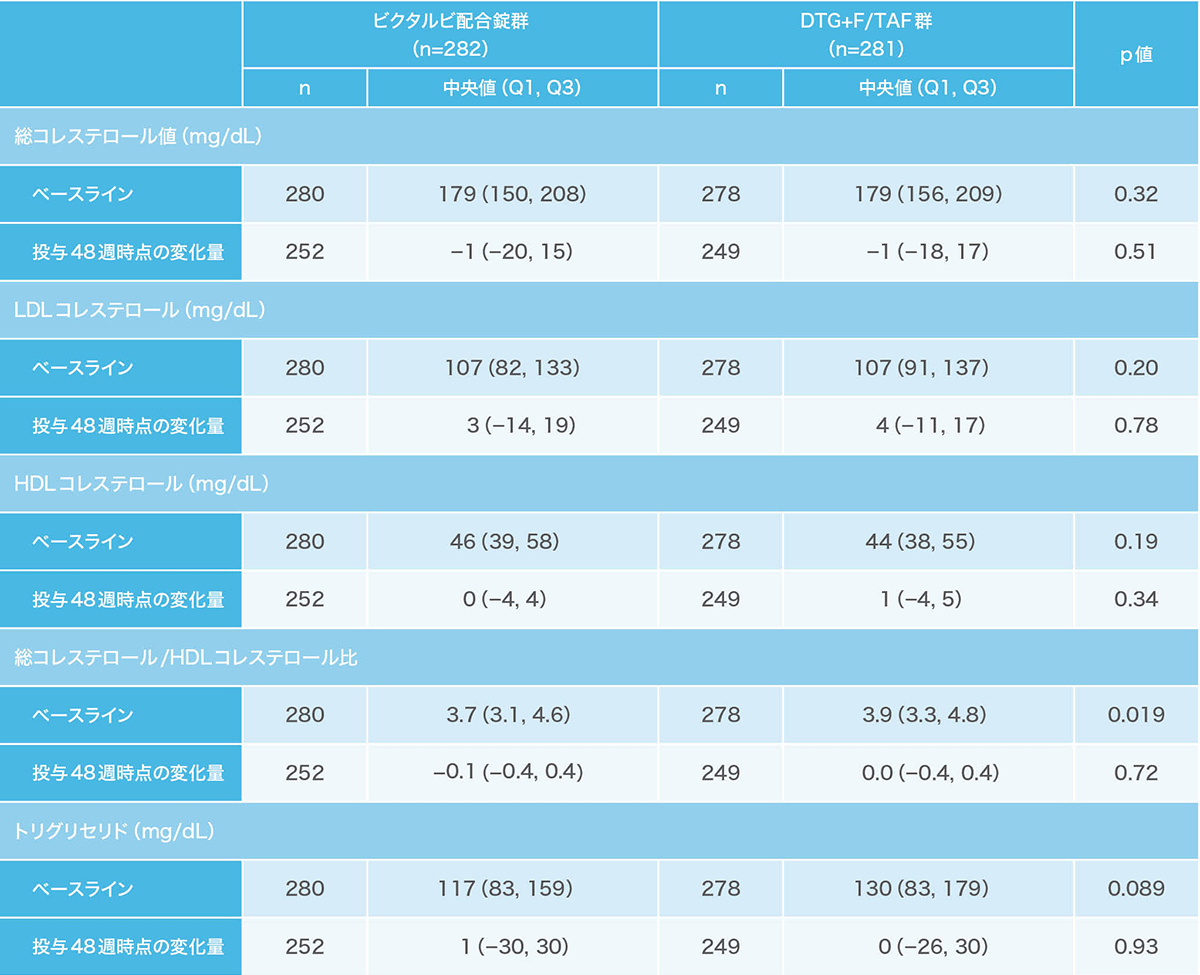
空腹時の臨床検査値のみをまとめた。LDLコレステロールは直接法による。
p値は両側ウィルコクソンの順位和検定による(ビクタルビ配合錠群 vs 対照群)。
ベースラインで脂質異常症治療薬を服用している被験者:ビクタルビ配合錠群 21%(59/284例)、DTG+F/TAF群 21%(60/281例)(p=0.92)
試験中に脂質異常症治療薬を開始した被験者:ビクタルビ配合錠群 5%(13/284例)、DTG+F/TAF群 3%(9/281例)(p=0.52)。
1: Sax PE, et al.: Clin Infec Dis 2021; 73(2): e485-e493.
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者、ギリアド・サイエンシズ社の社員である者が含まれます。







