292-1249試験(1249試験)(海外データ、国際共同治験)
抗HIV薬による治療経験がない又は抗HIV薬によりウイルス学的抑制が得られている 成人HIV-1/HBV重複感染症患者
HIV-1/HBV重複感染の成人患者を対象とした、ゲンボイヤ配合錠の有効性及び安全性試験
・Gilead社:社内資料 292-1249試験[承認時評価資料]
・Gallant J. et al.: J Acquir Immune Defic Syndr. 73 (3) : 294-298, 2016.
〔利益相反〕本研究はGilead社の資金により実施された。
試験概要
試験の概要は以下のとおりです。
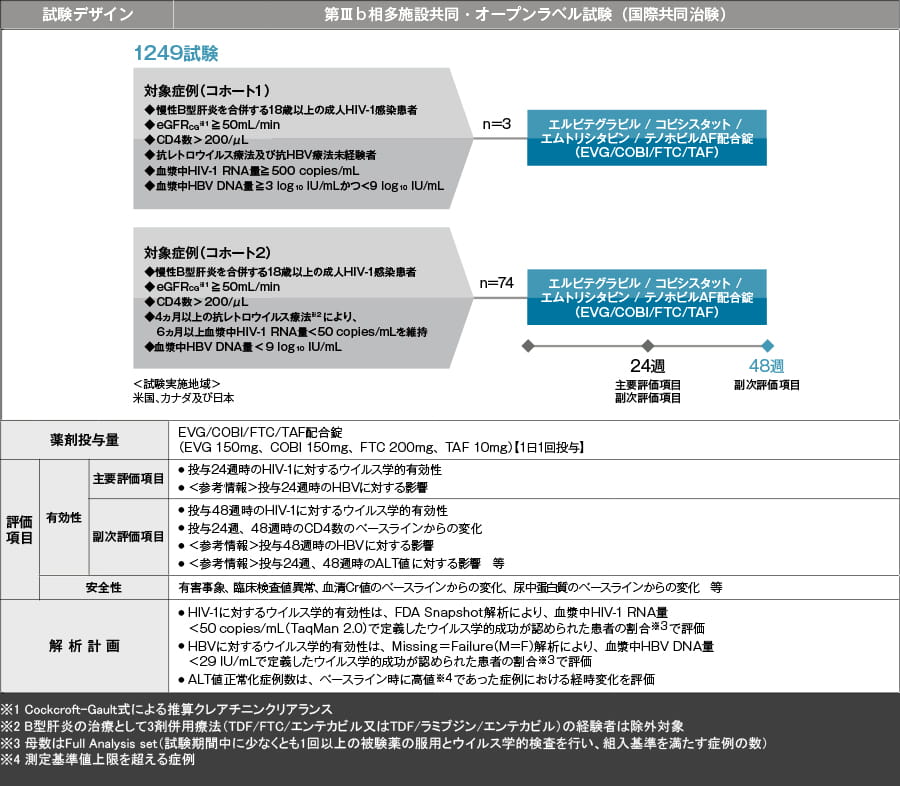
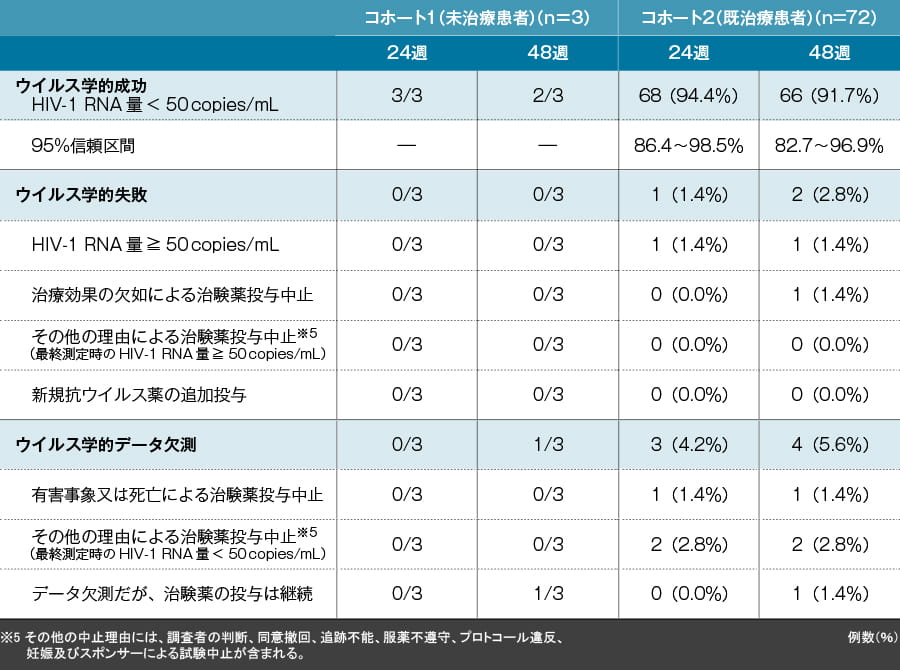
HIV-1に対するウイルス学的効果:FDA Snapshot解析(24週【主要評価項目】、48週【副次評価項目】)
投与後24週及び48週時の血漿中HIV-1 RNA量が50 copies/mL未満でウイルス学的有効性が認められた症例は、コホート1ではそれぞれ3例中3例及び3例中2例、コホート2ではそれぞれ94.4%及び91.7%でした。
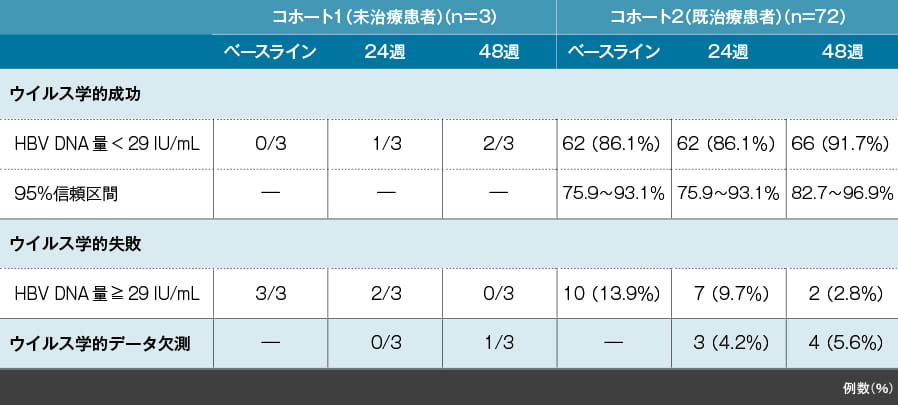
<参考情報> HBVに対する影響:M=F解析(24週【主要評価項目】、48週【副次評価項目】)
投与後24週及び48週時の血漿中HBV DNA量が29 IU/mL未満であった症例は、コホート1ではそれぞれ3例中1例及び3例中2例、コホート2ではそれぞれ86.1%及び91.7%でした。
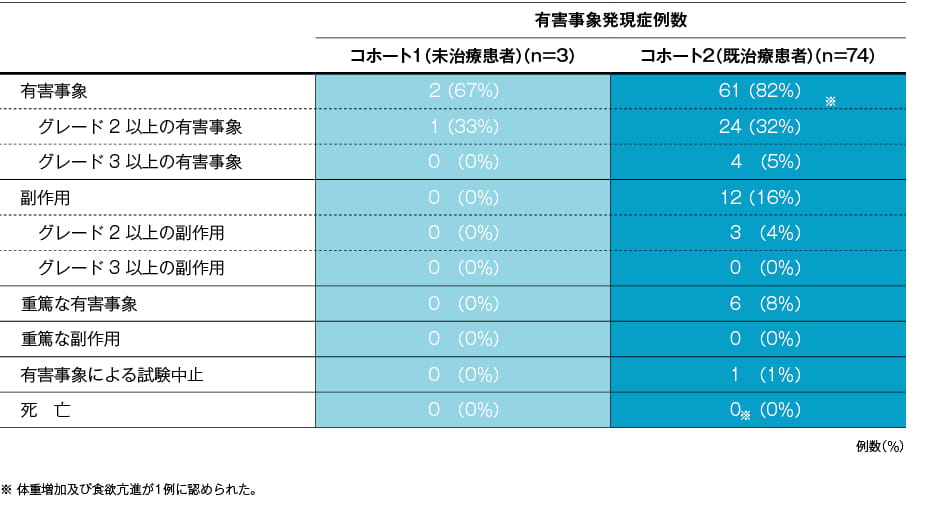
有害事象/臨床検査値異常
投与48週までの有害事象とその内訳及びグレード3又は4の臨床検査値異常を以下に示します。
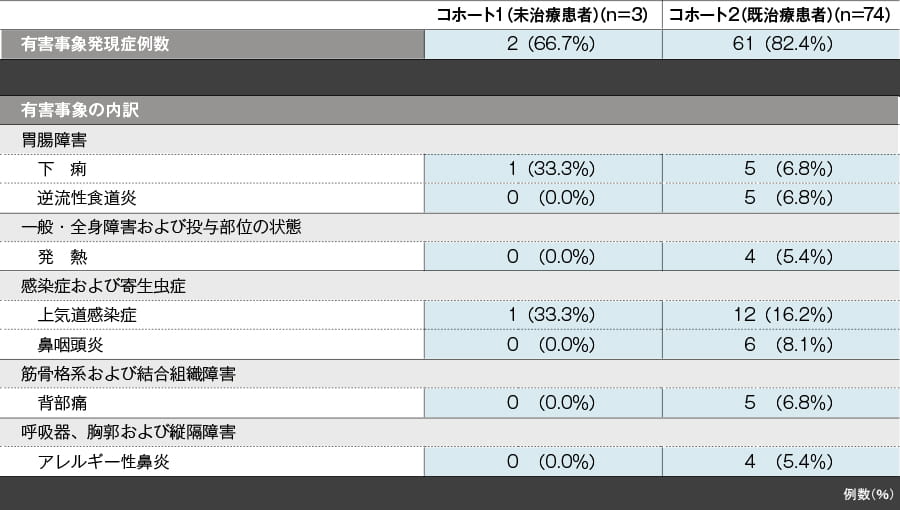
(1)有害事象(48週【副次評価項目】)
(2)コホート2で5%以上発現した有害事象(48週【副次評価項目】)
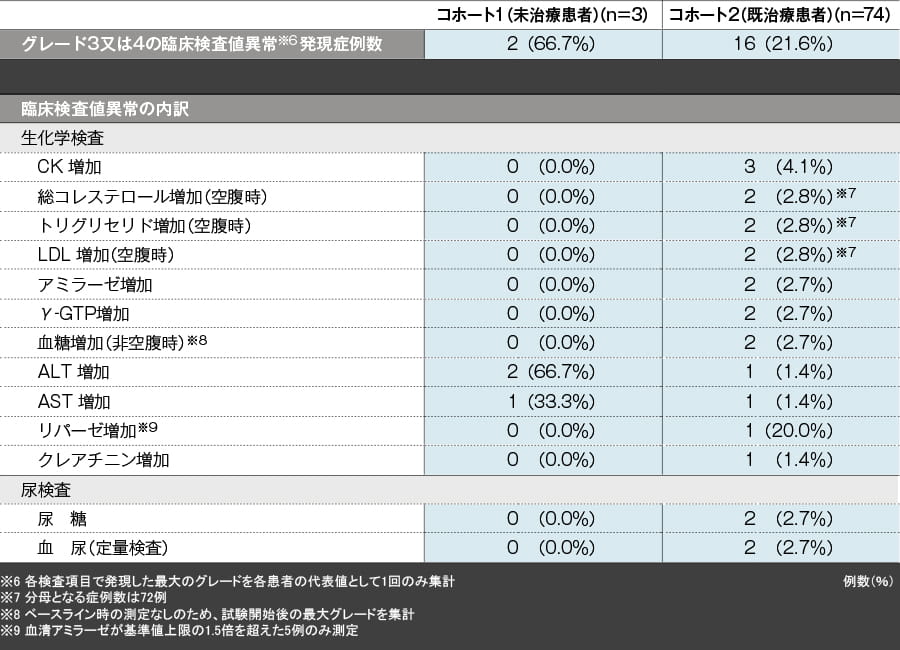
(3)グレード3又は4の臨床検査値異常(48週【副次評価項目】)
【効能・効果】
HIV-1感染症







