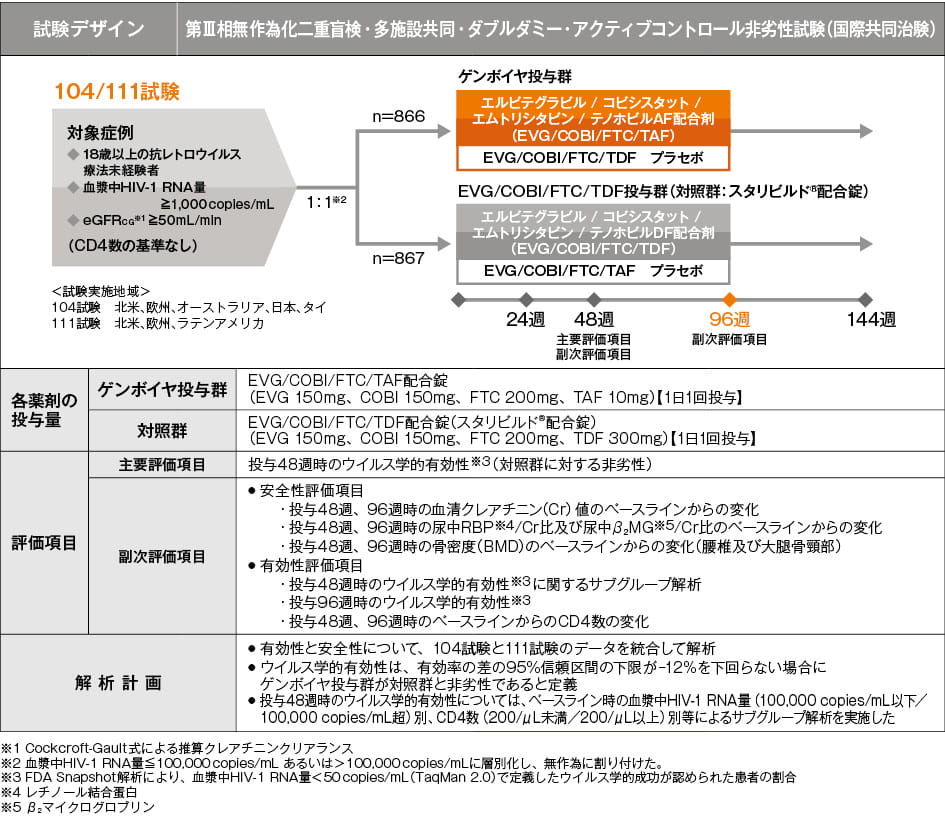
292-0104/0111試験(104/111試験)(海外データ、国際共同治験)
抗HIV薬による治療経験がないHIV-1感染症患者
ゲンボイヤ配合錠とスタリビルド配合錠(EVG/COBI/FTC/TDF)との非劣性試験
・Gilead社:社内資料 292-0104/0111試験[承認時評価資料]
・Sax P.E. et al. : Lancet 385(9987):2606-2615, 2015.
・Wohl D. et al. : J Acquir Immune Defic Syndr. 72(1):58-64, 2016.
〔利益相反〕 本研究はGilead社の資金により実施された。
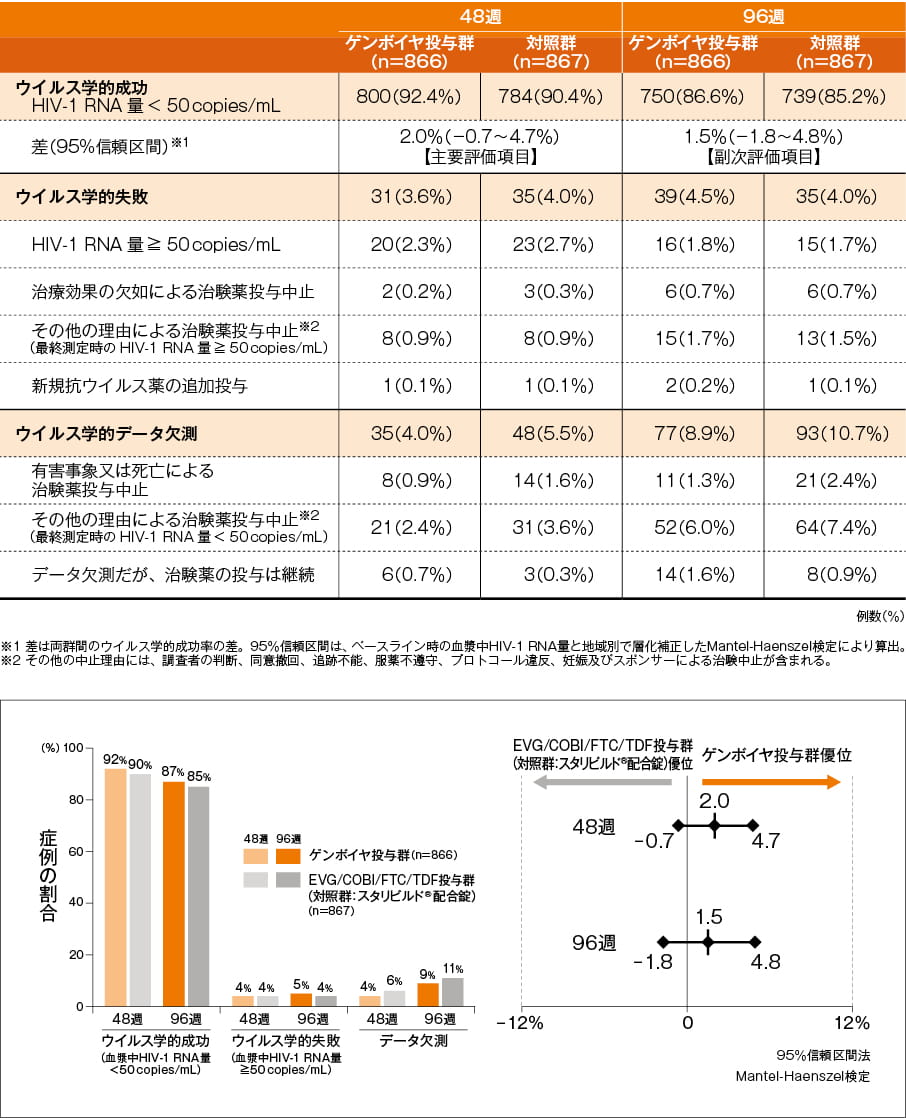
ウイルス学的効果:FDA Snapshot解析(48週【主要評価項目】、96週【副次評価項目】)
主要評価項目である投与48週の血漿中HIV-1 RNA量が50 copies/mL未満でウイルス学的有効性が認められた患者の比率は、ゲンボイヤ投与群で92.4%、対照群で90.4%、有効率の差は2.0%(95%信頼区間:-0.7~4.7%)であり、事前に設定した非劣性の基準(95%信頼区間の下限が-12%を下回らない場合)を満たしたことから、ゲンボイヤ投与群は対照群に対し非劣性であることが示されました。
有害事象/臨床検査値異常
投与96週までの有害事象とその内訳及びグレード3又は4の臨床検査値異常を以下に示します。
(1)有害事象(96週)
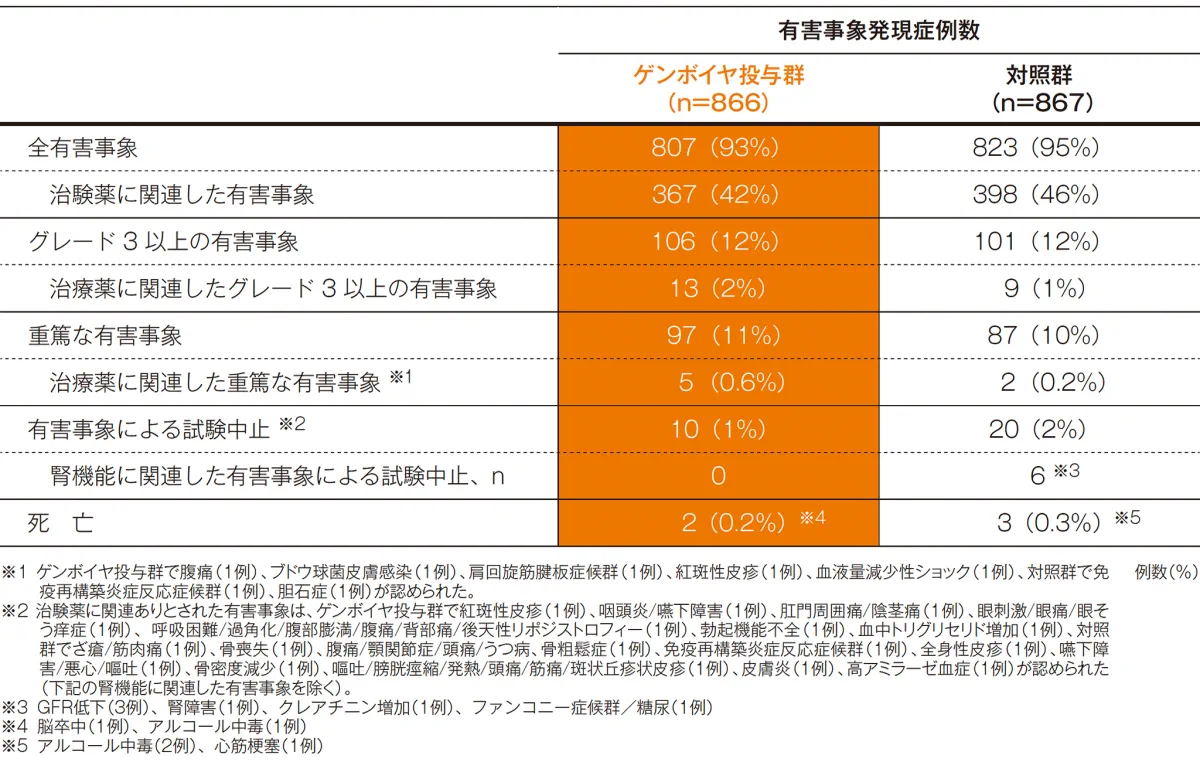
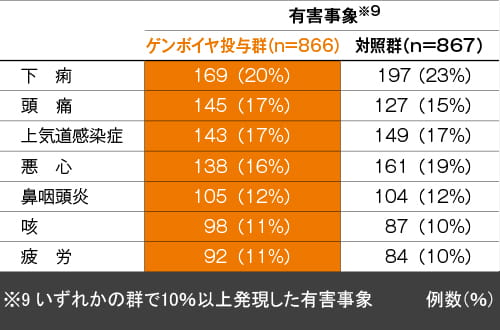
(2)有害事象の内訳(96週)
(3)臨床検査値異常の内訳(96週)