1489/1489試験のOLE 安全性(海外データ)
第Ⅲ相国際共同試験(1489/1490試験のOLE):投与開始240週時までの治療薬との関連が否定できない有害事象等(その他の評価項目)(海外データ)
HIV-1感染症未治療患者を対象とした1489試験および1490試験のOLEにおける、ビクタルビの副作用による投与中止率は240週を通して0.8%でした。

Sax PE, et al.: eClinicalMedicine 2023; 59: 101991.
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者、ギリアド・サイエンシズ社の社員である者が含まれます。
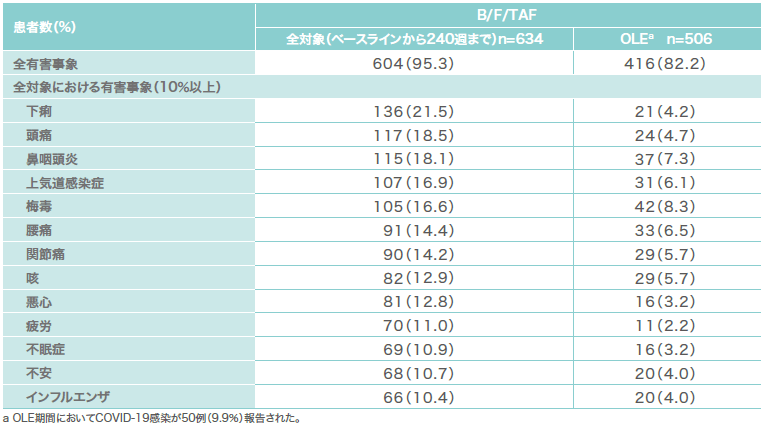
第Ⅲ相国際共同試験(1489/1490試験のOLE):投与開始240週時までの有害事象の発現状況および10%以上の有害事象(その他の評価項目)(海外データ)
HIV-1感染症未治療患者を対象とした1489試験および1490試験のOLEにおける有害事象は240週を通して95.3%、OLE期間では82.2%でした。
Sax PE, et al.: eClinicalMedicine 2023; 59: 101991.
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者、ギリアド・サイエンシズ社の社員である者が含まれます。
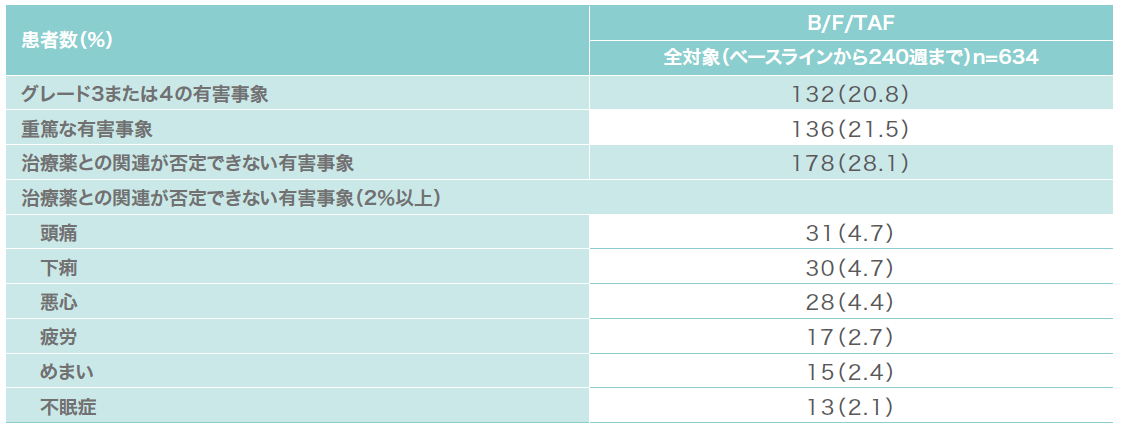
第Ⅲ相国際共同試験(1489/1490試験のOLE):投与開始240週時までのグレード3または4の有害事象の発現状況および治療薬との2%以上の有害事象(その他の評価項目)(海外データ)
HIV-1感染症未治療患者を対象とした1489試験および1490試験のOLEにおけるグレード3または4の有害事象は240週を通して20.8%でした。
Sax PE, et al.: eClinicalMedicine 2023; 59: 101991.
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者、ギリアド・サイエンシズ社の社員である者が含まれます。
第Ⅲ相国際共同試験(1489/1490試験のOLE):投与開始240週時までの臨床検査値異常の発現状況(その他の評価項目)(海外データ)
抗HIV薬による治療経験がないHIV-1感染症患者を対象とした1489試験および1490試験のOLEにおけるベースライン時から投与開始240週時までの臨床検査値異常の発現状況

Sax PE, et al.: eClinicalMedicine 2023; 59: 101991. より作図
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者、ギリアド・サイエンシズ社の社員である者が含まれます。
第Ⅲ相国際共同試験(1489/1490試験のOLE):【参考情報】ベースライン時から投与開始240週時までのeGFRCGの変化量の推移(その他の評価項目)(海外データ)
eGFRCGは試験初期に-12.0の低下を示した後、240週までの変化量の中央値は、評価時点で-5.8~-8.8で推移しました。
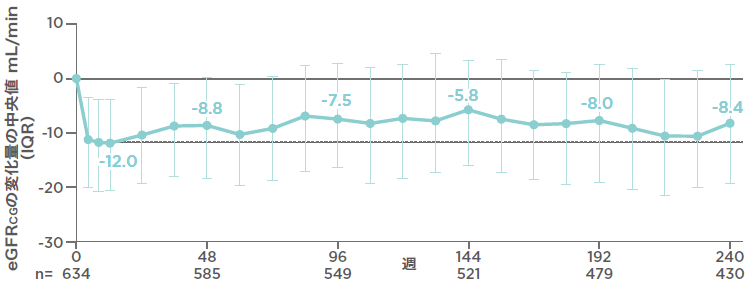
240週間のB/F/TAF投与を通じて、2635.6人年の追跡期間中、近位腎尿細管障害や腎臓の有害事象による中止の報告はありませんでした(発生率:100人年あたり0、95%CI:0-0.140)。
Sax PE, et al.: eClinicalMedicine 2023; 59: 101991.
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者、ギリアド・サイエンシズ社の社員である者が含まれます。
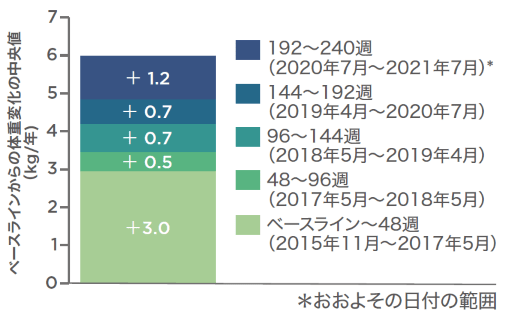
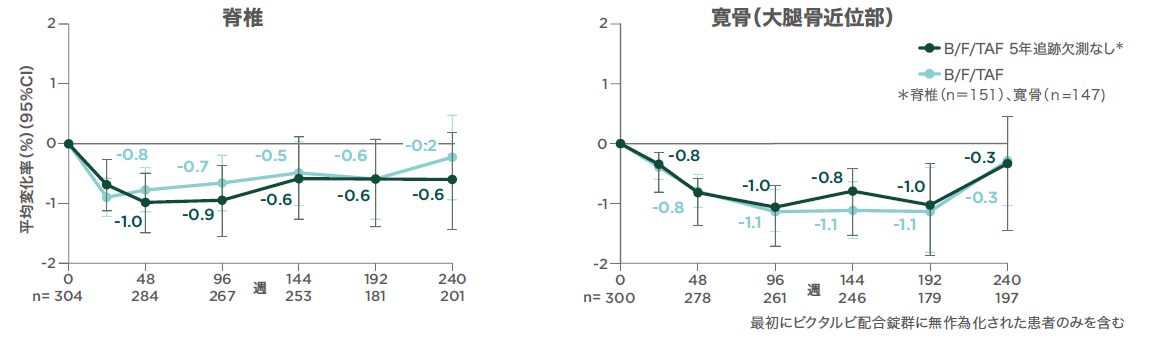
第Ⅲ相国際共同試験(1489試験のOLE):【参考情報】脊椎および寛骨(大腿骨近位部)の骨密度のベースラインからの平均変化率(その他の評価項目)(海外データ)
骨密度の5年間の平均減少率は脊椎で0.23%、股関節で0.29%でした。
Sax PE, et al.: eClinicalMedicine 2023; 59: 101991.
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者、ギリアド・サイエンシズ社の社員である者が含まれます。
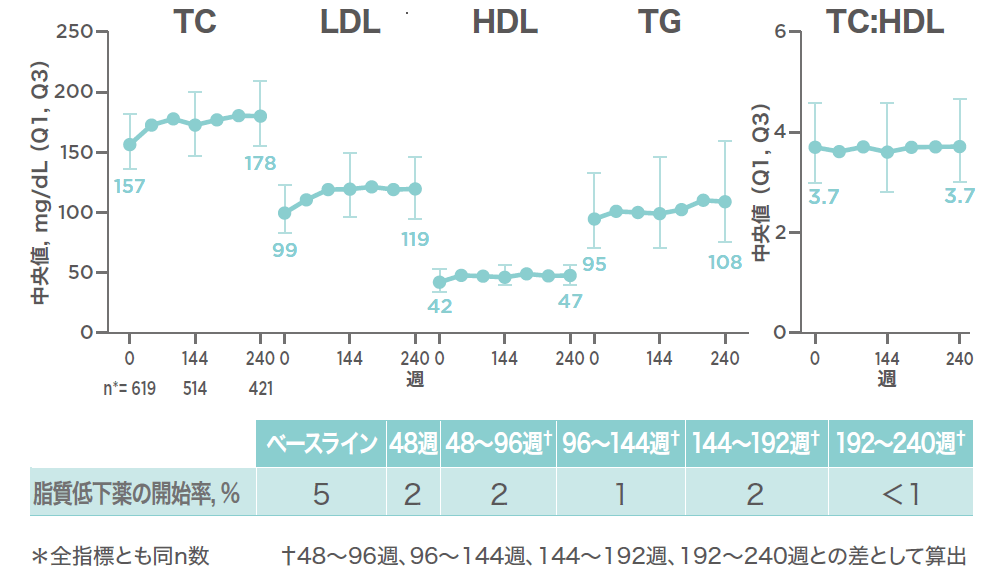
第Ⅲ相国際共同試験(1489/1490試験のOLE):【参考情報】ベースライン時から投与開始240週時までの空腹時脂質値の変化の中央値(その他の評価項目)(海外データ)
ベースライン時から投与開始240週時までの空腹時脂質値の変化の中央値の範囲は0~21mg/dLで、脂質低下薬を開始したのは、<1~5%でした。
Sax PE, et al.: eClinicalMedicine 2023; 59: 101991.
本試験はギリアド・サイエンシズ社より支援を受けています。著者にギリアド・サイエンシズ社より支援を受けている者、ギリアド・サイエンシズ社の社員である者が含まれます。